Immunosuppressiva en tyrosinekinaseremmers: retrospectief onderzoek naar een potentiële geneesmiddelinteractie
- Rubriek: Korte bijdrage
- Identificatie: 2023;8:a1768
Kernpunten
- Er is weinig bekend over eventuele interacties tussen combinaties van immunosuppressiva en tyrosinekinaseremmers (TKI’s).
- Bij combinatie van immunosuppressiva met ruxolitinib is op voorhand geen dosisaanpassing nodig bij start van de TKI.
- Monitoring van bloedspiegels van het immunosuppressivum blijft noodzakelijk in verband met de smalle therapeutische breedte en grote inter- en intra-individuele variatie in farmacokinetiek.
Abstract
Immunosuppressant drugs and tyrosine kinase inhibitors: a potential drug-drug interaction
Background
A possible interaction was seen in daily practice between immunosuppressant drugs and tyrosine kinase inhibitors (TKIs). A patient appeared to have high blood levels of the immunosuppressant drugs while using a TKI. This may lead to side effects, toxicity and even hospital admission.
It is unknown if there are interactions between immunosuppressant drugs based on literature. Possible mechanisms of the drug-drug interaction are cytochrome P450 (CYP) inhibition or induction or P-glycoprotein (PgP) inhibition or induction by the TKI which causes altered metabolism of the immunosuppressant drugs.
Objective
The aim of this study was to investigate drug-drug interactions between immunosuppressant drugs and TKIs leading to changes in immunosuppressant blood levels.
Design
Hypothesis generating retrospective study.
Methods
Patients treated at our hospital between January 2018 and July 2021 were selected from our electronic medical record. We included patients that used immunosuppressant drugs and started using a TKI. Blood levels needed to be measured before start of the TKI or after use of the TKI and during treatment with the TKI. The dose corrected blood levels in presence of the TKI were compared with the levels without use of the TKI.
Results
51 patients were included in the study, 8 immunosuppressant TKI combinations were studied. The majority of these patients used a combination of an immunosuppressant drug and ruxolitinib. No statistically significant changes were observed in immunosuppressant blood levels related to the use of ruxolitinib.
Conclusion
No dose adjustments of immunosuppressant drugs are needed at the start of therapy with ruxolitinib. Therapeutic drug monitoring of the immunosuppressant drugs remains important to optimize therapy in these patients.
Inleiding
Immunosuppressiva worden gebruikt ter voorkoming van afstoting na orgaantransplantatie. Omdat deze geneesmiddelen een smal therapeutisch venster hebben en een grote inter- en intra-individuele variatie in de farmacokinetiek, wordt therapeutic drug monitoring (TDM) toegepast om de dosering te individualiseren. Een van de factoren die de blootstelling van een immunosuppressivum beïnvloedt, is het optreden van geneesmiddelinteracties [1]. Tyrosinekinaseremmers (TKI’s) worden gebruikt bij de behandeling van patiënten met kanker. In de dagelijkse praktijk in ons ziekenhuis werd een casus gezien met een mogelijke geneesmiddelinteractie tussen een immunosuppressivum en een TKI. Deze patiënt had een sterke stijging van de tacrolimusspiegel tot toxische waarden bij gebruik van crizotinib. Hoge immunosuppressivaspiegels kunnen leiden tot toxiciteit zoals een verminderde nierfunctie en tot een ziekenhuisopname [1].
Vanuit de literatuur is onvoldoende bekend over interacties tussen immunosuppressiva en TKI’s. Er is een interactie beschreven tussen imatinib en ciclosporine en tussen dasatinib, nilotinib en imatinib en de immunosuppressiva tacrolimus, sirolimus, ciclosporine en everolimus [2-4]. Over eventuele interacties tussen andere combinaties van immunosuppressiva en TKI’s is weinig bekend. Mogelijke mechanismen van geneesmiddelinteracties door TKI’s zijn remming of inductie van Cytochroom P450 (CYP)-enzymen of remming of inductie van P-glycoproteïne (PgP), wat zorgt voor een verandering van de farmacokinetiek van het immunosuppressivum, omdat deze substraten zijn voor de genoemde enzymen [5-9]. Bij een verandering in farmacokinetiek ten gevolge van een interactie kan het nodig zijn om de dosis van het immunosuppressivum aan te passen om afstoting of toxiciteit te voorkomen. Informatie over interacties tussen deze geneesmiddelengroepen helpt artsen en apothekers in de dagelijkse praktijk bij de behandeling van de patiënt. Op basis van de aanwijzingen vanuit de literatuur, aangevuld met onze eerdere casus, werd geconstateerd dat er mogelijk een interactie speelt tussen immunosuppressiva en TKI’s, maar dat de mate en klinische relevantie onduidelijk is. Het doel van dit onderzoek was het effect van het gebruik van TKI’s op de bloedspiegels van immunosuppressiva te onderzoeken.
Methoden
Een hypothese genererend retrospectief cohortonderzoek werd uitgevoerd in het Universitair Medisch Centrum Groningen (UMCG). Patiënten werden geselecteerd vanuit het elektronisch patiëntendossier Epic middels de rapportagemodule SlicerDicer. Patiënten ouder dan 18 jaar die werden behandeld in het ziekenhuis (zowel opgenomen als poliklinische patiënten) tussen 1 januari 2018 en 1 juli 2021 en die een medicatievoorschrift hadden voor een immunosuppressivum (ciclosporine, tacrolimus, everolimus of sirolimus) en een TKI, en waarvoor een bloedspiegel van een van deze immunosuppressiva is gemeten, werden gescreend voor inclusie. Patiënten werden geïncludeerd wanneer ze gelijktijdig een immunosuppressivum en een TKI gebruikten, er ook een episode was waarin de patiënt alleen het immunosuppressivum gebruikte en er bloedspiegels waren bepaald voor aanvang van de TKI of na staken van de TKI en tijdens het gebruik van de TKI. Patiënten werden geëxcludeerd wanneer zij hadden aangegeven geen toestemming te geven voor dataverzameling. Dit onderzoek werd uitgevoerd na goedkeuring van de Medisch Ethische Toetsingscommissie (METc). Vanwege het retrospectieve karakter van dit onderzoek werd door de METc dispensatie verleend voor het vragen van informed consent aan de patiënten. Per combinatie van een immunosuppressivum en een TKI werden maximaal 25 patiënten geïncludeerd.
De patiëntkarakteristieken (geslacht, leeftijd, lengte, gewicht, comorbiditeit, gegevens over de transplantatie, CYP genotype, nierfunctie, leverfunctie), gegevens over het medicatiegebruik en bloedspiegels tijdens en 1 maand voorafgaand of na gebruik van de TKI werden handmatig verzameld uit het patiëntendossier en gedocumenteerd in het electronic Case Report Form (eCRF) in de Research Electronic Data capture database (RedCap). In verband met de handmatige dataverzameling en -invoer, is een steekproefsgewijze controle geweest door een tweede persoon.
De concentratie/dosis (C/D)-ratio werd berekend bij elke gemeten spiegel. Deze werd berekend door de gemeten plasmaconcentratie van het immunosuppressivum te delen door de dagdosis van het immunosuppressivum. Van elke patiënt werd een grafiek gemaakt van het verloop van de C/D-ratio in de tijd om een verandering van de C/D-ratio in kaart te brengen. De C/D-ratio van het immunosuppressivum tijdens het gebruik van de TKI werd vergeleken middels een Wilcoxon-rangsomtoets met de ratio zonder het gebruik van de TKI. De statistische analyses zijn uitgevoerd in IBM SPSS Statistics (versie 28). Wanneer een immunosuppressivum zowel oraal als intraveneus werd gebruikt, dan zijn deze toedienroutes gescheiden in de analyse omdat de biologische beschikbaarheid invloed heeft op de gevonden C/D-ratio.
Resultaten
Van de 215 gescreende patiënten waren 79 patiënten geschikt voor inclusie. Van deze 79 patiënten zijn 51 patiënten geïncludeerd in het onderzoek. De overige geïncludeerde patiënten gebruikten een combinatie van tacrolimus en ruxolitinib. Van deze geneesmiddelencombinatie waren reeds 25 patiënten geïncludeerd (figuur 1). De patiëntkarakteristieken van de geïncludeerde patiënten zijn weergegeven in tabel 1.
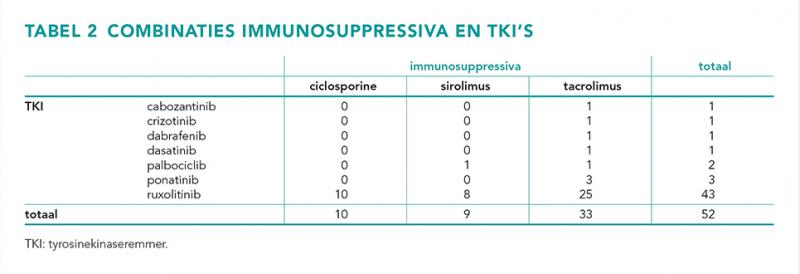
De combinaties immunosuppressivum + TKI die in de populatie werden gebruikt, zijn weergegeven in tabel 2. Het grootste gedeelte van de geïncludeerde patiënten (25 van de 51) gebruikte een combinatie van tacrolimus en ruxolitinib na een allogene stamceltransplantatie, waarbij de patiënt ‘graft versus host’-ziekte ontwikkelde.
De gemiddelde C/D-ratio van oraal tacrolimus steeg na start van ruxolitinib met 66% van 2,5 (± 1,7) μg/L/mg naar 4,1 (± 2,5) μg/L/mg (P = 0,07) en daalde na staken van ruxolitinib ongeveer weer terug naar de uitgangswaarde 2,3 (± 1,1) μg/L/mg (figuur 2A). De gemiddelde C/D-ratio van intraveneus tacrolimus steeg van 9,2 (± 5,1) μg/L/mg naar 16,6 (± 4,7) μg/L/mg (P = 0,07) na start van ruxolitinib. Na staken van ruxolitinib daalde de gemiddelde C/D-ratio niet, maar bleef op hetzelfde niveau (17,8 ± 3,5 μg/L/mg) (P = 1,00; figuur 2B). Uitgedrukt in percentages steeg de C/D-ratio gemiddeld tot 180% na start van tacrolimus intraveneus en was na staken 193% van de uitgangswaarde.
Om het effect van comedicatie op de C/D-ratio uit te sluiten, is ook de analyse uitgevoerd waarbij spiegels die waren gemeten op een moment dat de patiënt een triazoolderivaat (fluconazol, voriconazol, posaconazol) gebruikte zijn verwijderd uit de analyse. Het resultaat hiervan is weergegeven in figuur 2C en 2D. De gemiddelde C/D-ratio van oraal tacrolimus steeg met 58% na start van ruxolitinib van 2,1 (± 1,5) μg/L/mg naar 3,3 (± 2,7) μg/L/mg (P = 0,37). Na staken van ruxolitinib daalde de gemiddelde C/D-ratio weer naar 2,4 (± 1,2) μg/L/mg (P = 0,20). Bij intraveneus toegediend tacrolimus steeg de gemiddelde C/D-ratio van 9,9 (± 0,8) μg/L/mg naar 17,1 (± 2,8) μg/L/mg (P = 0,25), een stijging van gemiddeld 72%. Na staken van de ruxolitinib daalde de tacrolimus C/D-ratio niet weer terug naar de uitgangswaarde, maar bleef gemiddeld 17,2 (± 3,4) μg/L/mg (P = 0,50). De tacrolimus C/D-ratio voor, gedurende en na gebruik van ruxolitinib is niet significant verschillend.
In figuur 3 is te zien dat er een grote variatie was in de stijging in de tacrolimus C/D-ratio tussen patiënten. Met name bij drie patiënten is een grote stijging in de C/D-ratio te zien tijdens het gebruik van ruxolitinib.
Bij de combinatie ciclosporine + ruxolitinib en de combinatie sirolimus + ruxolitinib wordt dezelfde trend gezien. Ook hier zijn geen significante verschillen in de C/D-ratio gevonden zonder en met gebruik van ruxolitinib (figuur 4 en 5).
Bij de overige combinaties immunosuppressivum + TKI werden geen opvallende verschillen gezien in de C/D-ratio tussen de periode met gebruik van een TKI en zonder gebruik van de TKI. Bij de combinatie tacrolimus + crizotinib werd een sterke stijging in de tacrolimus C/D-ratio gezien bij combinatie met crizotinib (figuur 6). Deze stijging in C/D-ratio trad echter pas op meer dan 50 dagen na start van crizotinib. Voor deze stijging startte de patiënt met behandeling met voriconazol.
Beschouwing
Dit onderzoek betreft een retrospectief hypothese genererend cohortonderzoek. Middels dit type onderzoek is het mogelijk om een grote groep patiënten te onderzoeken die een bepaalde geneesmiddelencombinatie gebruikt. Omdat TKI’s veel worden gebruikt in de (hemato)oncologie en deze geneesmiddelen interacties kunnen hebben met andere geneesmiddelen, is het van belang om te weten of deze geneesmiddelen veilig kunnen worden gecombineerd. In dit onderzoek is geen eenduidige interactie gevonden tussen immunosuppressiva en ruxolitinib, die gemiddeld een statistisch significant effect had op de immunosuppressivaspiegel in de onderzochte populatie. De individuele variatie in het verloop van de bloedspiegels van de immunosuppressiva is echter wel groot tijdens en na het gebruik van ruxolitinib. Daarom is een nauwgezette monitoring van de tacrolimusspiegels tijdens en na het gebruik van ruxolitinib van belang voor een optimale en veilige behandeling.
Genotype is een onderdeel van deze interindividuele variatie, echter was van geen van de geïncludeerde patiënten een CYP-genotypering bekend. Bij drie patiënten was een sterke stijging in de C/D-ratio gevonden na start van ruxolitinib. In de tijd kunnen factoren als C-reactief proteïne (CRP), diarree en leverfunctie van de patiënt van invloed zijn op de immunosuppressivaspiegels [10]. Ook kan één hoge spiegel een grote invloed hebben op de gemiddelde C/D-ratio van een patiënt. Uit de verzamelde gegevens blijkt geen duidelijk gemeenschappelijke oorzaak van de stijging van de tacrolimusspiegel bij deze patiënten. Op basis van gevonden resultaten lijkt op voorhand geen dosisaanpassing nodig van een immunosuppressivum bij start van ruxolitinib. Over de overige onderzochte combinaties immunosuppressivum + TKI kan geen eenduidige conclusie worden getrokken gezien de kleine patiëntenaantallen.
Doordat dit een retrospectief onderzoek betreft met een beperkte patiëntenpopulatie, is slechts een beperkt aantal combinaties van immunosuppressiva + TKI’s onderzocht. We hebben in dit onderzoek wel de meest gebruikte geneesmiddelencombinaties onderzocht. De grootste groep patiënten gebruikte een combinatie van ruxolitinib met een immunosuppressivum in het kader van de behandeling van ‘graft versus host’-ziekte na een allogene stamceltransplantatie. Om een interactie tussen andere TKI’s en immunosuppressiva uit te sluiten is verder onderzoek nodig, bij voorkeur in een prospectief onderzoek waarbij de invloed van comedicatie, farmacogenetica en intra-individuele variatie op de immunosuppressivaspiegels zo veel mogelijk wordt beperkt. Er bestaat een risico dat de verzamelde gegevens onjuist of onvolledig waren omdat de data is verzameld uit de patiëntendossiers. Zorgverleners leggen niet altijd adequaat de medicatiegegevens van patiënten vast. Daarnaast gebruikten de patiënten veel verschillende geneesmiddelen waardoor het lastig is om het effect van de TKI op de immunosuppressivaspiegels geïsoleerd te bekijken. Bij de onderzoeksopzet is ervoor gekozen om maximaal 25 patiënten per combinatie TKI + immunosuppressivum te includeren. De verwachting was dat indien een significant klinisch relevante interactie is bij de combinatie van geneesmiddelen, deze duidelijk naar voren zou komen in de analyse. Om uit te sluiten dat door ontbreken van de betreffende gegevens een mogelijke interactie is gemist, zullen deze aanvullende data nog worden verzameld voor verdere analyse.
De gepubliceerde interactie tussen dasatinib en tacrolimus, waarbij de blootstelling van tacrolimus toeneemt [4], kon niet bevestigd worden in dit onderzoek. Slechts één patiënt in dit onderzoek gebruikte deze combinatie.
Conclusie
Bij combinatie van immunosuppressiva met ruxolitinib is op voorhand geen dosisaanpassing nodig van het immunosuppressivum bij start van ruxolitinib. Over de overige onderzochte combinaties immunosuppressivum + TKI kan geen eenduidige conclusie worden getrokken gezien de kleine patiëntenaantallen. Monitoring van bloedspiegels van het immunosuppressivum blijft noodzakelijk in verband met de smalle therapeutische breedte en grote inter- en intra-individuele variatie in farmacokinetiek.
Verantwoording
Geen belangenverstrengeling gemeld.
Literatuur
1. Brunet M, van Gelder T, Åsberg A, et al. Therapeutic Drug Monitoring of Tacrolimus-Personalized Therapy: Second Consensus Report. Ther Drug Monit. 2019;41(3):261–307.
2. Atiq F, Broers AE, Andrews L, et al. A clinically relevant pharmacokinetic interaction between cyclosporine and imatinib. Eur J Clin Pharmacol. 2016;72(6):719-723.
3. Onaka T, Takahashi N, Miura M, Yonezawa A. Drug interaction between tacrolimus and nilotinib in a patient with chronic myeloid leukemia after renal transplant. Clin Case Rep. 2017;5(5):605–607.
4. Haouala A, Widmer N, Duchosal MA, Montemurro M, Buclin T, Decosterd LA. Drug interactions with the tyrosine kinase inhibitors imatinib, dasatinib, and nilotinib. Blood. 2011;117(8):e75–e87.
5. Kirchner GI, Meier-Wiedenbach I, Manns MP. Clinical pharmacokinetics of everolimus. Clin Pharmacokinet. 2004;43(2):83–95.
6. Mahalati K, Kahan BD. Clinical pharmacokinetics of sirolimus. Clin Pharmacokinet. 2001;40(8):573–585.
7. Fahr A. Cyclosporin clinical pharmacokinetics. Clin Pharmacokinet. 1993;24(6):472–495.
8. Iwasaki K. Metabolism of tacrolimus (FK506) and recent topics in clinical pharmacokinetics. Drug Metab Pharmacokinet. 2007;22(5):328–335.
9. Hussaarts KGAM, Veerman GDM, Jansman FGA, van Gelder T, Mathijssen RHJ, van Leeuwen RWF. Clinically relevant drug interactions with multikinase inhibitors: a review. Ther Adv Med Oncol. 2019;11:1758835918818347.
10. Lenoir C, Daali Y, Rollason V, et al. Impact of Acute Inflammation on Cytochromes P450 Activity Assessed by the Geneva Cocktail. Clin Pharmacol Ther. 2021;109(6):1668–1676.
Referentie
Citeer als: Hofman S, Oude Munnink TH, Touw DJ, Lub-de Hooge MN. Immunosuppressiva en tyrosinekinaseremmers: retrospectief onderzoek naar een potentiële geneesmiddelinteractie. Nederlands Platform voor Farmaceutisch Onderzoek. 2023;8:a1768.
DOI
https://www.knmp.nl/resolveuid/1dba55056c2d47778adc3fc6a820aa45Open access








Reactie toevoegen