Geen nefrotoxiciteit na continue infusie amfotericine B met TDM bij ernstig zieke patiënten met abdominale sepsis
- Rubriek: Korte bijdrage
- Identificatie: 2021;6:a1746
Kernpunten
- Continu toegediend conventioneel amfotericine B met TDM leidt niet tot nefrotoxiciteit bij IC-patiënten.
- Geen van alle uitkomstmaten voor nefrotoxiciteit toont een relatie met continu toegediend conventioneel amfotericine B.
- Toepassing van continu conventioneel amfotericine B is goedkoper dan alternatieve antifungale geneesmiddelen.
Abstract
Nephrotoxicity of continuous infusion of amphotericin B in critically ill patients with abdominal sepsis
Background
Continuous infusion of conventional amphotericin B (CCAB) is used in intensive care units (ICUs) for pre-emptive treatment of invasive fungal infections. Conventional amphotericin B treatment has been associated with increased nephrotoxicity.
Objective
The aim of this retrospective multicenter cohort study is to investigate if CCAB with therapeutic drug monitoring (TDM) in critically ill patients results in impaired kidney function over time.
Design and methods
The study was conducted at mixed medical-surgical ICUs of two large teaching hospitals in the Netherlands. All consecutive patients who were admitted to the ICU and treated between 2006 and 2019 for abdominal infection were included.
Serum creatinine concentrations and renal failure scores of patients with CCAB treatment were compared with those without CCAB treatment. Excluded were patients treated with CCAB for less than 72 hours, patients treated for other reason than abdominal infection and patients with renal replacement therapy at the start of treatment.
Amphotericin B dosing was guided by TDM, with serum levels determined in the local hospital pharmacies (target serum levels 0.5-1.0 mg/L).
Results
A total of 319 patients were included, 185 treated with CCAB and 134 controls. A multiple linear regression model showed that the serum creatinine concentration was independent of CCAB treatment (β = −0.023; 95% confidence interval [CI] = −12.2-7.2; P = 0.615). Propensity score matching resulted in 134 pairs of CCAB treated and non-treated patients. The regression results including propensity score showed that the cumulative CCAB dose was not associated with creatinine concentration during intensive care treatment (β = 0.299; 95% CI = −0.38-0.98; P = 0.388).
Conclusion
This study demonstrates that CCAB with TDM did not result in renal impairment over time in critically ill patients.
Inleiding
Continue toediening van conventioneel amfotericine B (CCAB) wordt weinig toegepast op intensive cares (IC’s) vanwege mogelijk meer nefrotoxiciteit dan alternatieve antifungale therapieën [1]. CCAB kan op IC’s worden gebruikt bij kwetsbare patiëntgroepen met een verhoogd risico op invasieve schimmelinfecties [2]. Risicofactoren voor invasieve schimmelinfecties zijn bijvoorbeeld dragerschap met Candida of Aspergillus spp. [3], ernstige luchtweginfecties zoals influenza en COVID-19 [4], en abdominale sepsis bij secundaire peritonitis na darmperforatie [5]. Invasieve schimmelinfecties hebben een significante impact op mortaliteit en zorgkosten, waardoor pre-emptieve antifungale therapie is geïndiceerd [3,6-8].
Infusie van conventioneel amfotericine B (c-AmB) was meer dan 40 jaar de voorkeursbehandeling voor invasieve schimmelinfecties, maar gerapporteerde nefrotoxiciteit na toediening van intermitterende amfotericine B zorgde voor een overstap naar liposomaal amfotericine B en echinocandinen in behandelrichtlijnen [9-17]. CCAB vertoont echter minder nefrotoxiciteit dan c-AmB en nierinsufficiëntie is mild en omkeerbaar bij patiënten met acute myeloïde leukemie [18-20]. Door continue toepassing van amfotericine B worden hoge, potentieel nefrotoxische piekconcentraties voorkomen [18-20].
Amfotericine B kan worden toegepast als pre-emptieve antischimmeltherapie, bijvoorbeeld bij patiënten at risk voor invasieve schimmelinfecties zoals bij COVID-19 en gecompliceerd beloop na abdominale chirurgie, maar nefrotoxiciteit kan een reden zijn om hiermee terughoudend te zijn. Amfotericine B heeft een breed antifungaal spectrum en is goedkoper dan de meeste andere antifungale therapieën, waaronder lipidenformuleringen van amfotericine B, breedspectrumazolen en echinocandinen [19,21]. In deze studie onderzoeken wij of er een associatie is tussen nierfunctie en CCAB, specifiek ingezet als pre-emptieve therapie, met TDM bij IC-patiënten met abdominale sepsis.
Methoden
Ontwerp en populatie
Het onderzoek is een retrospectieve multicenter cohortstudie uitgevoerd op twee medisch-chirurgische IC’s in Nederland (OLVG Oost Amsterdam en Gelre ziekenhuis Apeldoorn). Alle patiënten die op deze IC’s tussen 2006 en 2019 werden opgenomen voor behandeling van abdominale sepsis werden geïncludeerd. Patiënten met CCAB-behandeling werden geselecteerd als CCAB-cohort en patiënten die geen antifungale therapie kregen als niet-CCAB-cohort. Patiënten die minder dan 72 uur met CCAB werden behandeld, patiënten die werden behandeld voor een andere infectie dan een abdominale sepsis en patiënten met nierfunctievervangende therapie bij aanvang werden geëxcludeerd. De lokale medisch-ethische toetsingscommissies beschouwden dit onderzoek als niet-WMO-plichtig.
Setting
CCAB wordt toegepast als pre-emptieve behandeling bij abdominale sepsis bij secundaire peritonitis na darmperforatie. In het Gelre ziekenhuis kregen alle patiënten met een gecompliceerd beloop na gastro-intestinale chirurgie CCAB. In OLVG werd de beslissing over het starten van CCAB-behandeling overgelaten aan de behandelend arts. Amfotericine B werd toegediend via een pompgedreven continue intraveneuze infusie via een centraal veneuze katheter, waarbij de dosering werd aangepast op basis van therapeutic drug monitoring (TDM). De serumconcentraties van amfotericine B werden bepaald in de lokale ziekenhuisapotheken met een gevalideerde ultra-high performance liquid chromatography-methode met massaspectrometrie (UHPLC-MS). De startdosering van amfotericine B was 0,7 mg/kg in OLVG en 0,5 mg/kg in het Gelre ziekenhuis en de referentiewaarden waren 0,5-1,0 mg/L in OLVG en 0,2-1,0 mg/L in het Gelre ziekenhuis [5].
Uitkomstmaten
Primaire uitkomstmaat was het verschil tussen de gemiddelde serumcreatinineconcentratie tijdens behandeling met amfotericine B (CCAB-cohort) of tijdens IC-opname (niet-CCAB-cohort) en de serumcreatinineconcentratie bij opname. Secundaire uitkomstmaten waren gevalideerde scores gerelateerd aan nierfalen: risk, injury, failure, loss of kidney function, end-stage kidney disease (RIFLE)-score, renale sequential organ failure assessment (SOFA)-score en de fractie patiënten die continue venoveneuze hemodialyse (CVVHD) nodig hadden [22].
Data-analyse
Data werden geëxtraheerd uit de lokale IC-databases Metavision (Tel Aviv, Israël). Laboratoriumwaarden werden routinematig dagelijks om 06.00 uur bepaald. Indien deze bij opname niet beschikbaar waren, werden de waarden van de dag voor of na opname gebruikt.
De ongepaarde t-toets, Mann-Whitneytoets, Fischer-exacttoets en de chi-kwadraattoets werden gebruikt voor het weergeven van de basiskarakteristieken. Univariate lineaire regressieanalyses werden uitgevoerd met de primaire en secundaire uitkomstmaten als afhankelijke variabelen. Multipele lineaire regressie met standaardselectie werd uitgevoerd met de primaire uitkomstmaat als afhankelijke variabele. Leeftijd, serumcreatinineconcentratie en acute physiology and chronic health evaluation (APACHE) III-score werden op klinische gronden aangemerkt als voorspellers voor CCAB-behandeling. Deze variabelen werden daarom als onafhankelijke variabelen toegevoegd aan het model.
Een propensity score matching werd uitgevoerd om te corrigeren voor mogelijke confounding [23]. Deze score berekent de kans op het krijgen van CCAB-behandeling [24], waarbij leeftijd, APACHE III-score en serumcreatinineconcentratie bij aanvang als potentiële voorspellers
zijn meegenomen. Behandelde personen werden 1:1 gematcht met onbehandelde personen met een matchtolerantie van 0,1.
Alle statistische analyses werden uitgevoerd met behulp van het Statistical Package for the Social Science (SPSS) versie 26.0 (SPSS Inc., Chicago Illinois). Een tweezijdige alfa van 5% werd als significantieniveau genomen [23].
Resultaten
Figuur 1 toont het stroomdiagram van de geïncludeerde en geëxcludeerde patiënten. Er werden 319 patiënten met abdominale sepsis geïncludeerd, waarvan 185 patiënten (respectievelijk 96 in OLVG en 89 patiënten in het Gelre ziekenhuis) werden behandeld met CCAB en 134 patiënten (allen OLVG-patiënten) in het niet-CCAB cohort.
Patiëntkarakteristieken zijn weergegeven in tabel 1. De niet-CCAB-groep was jonger, minder ernstig ziek en de diurese bij aanvang was hoger. Er waren geen verschillen tussen beide groepen wat betreft nefrotoxische comedicatie, zoals vancomycine.
Primaire uitkomst
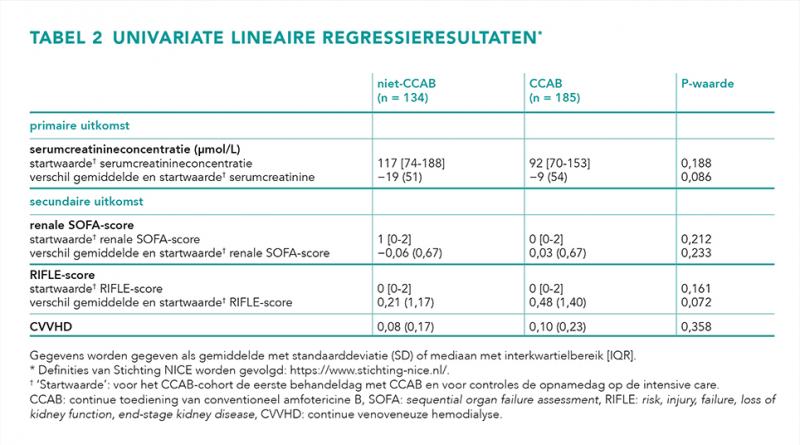
Univariate regressieresultaten van de 319 geïncludeerde patiënten zijn weergegeven in tabel 2. Er waren geen significante verschillen te zien tussen beide cohorten in de primaire uitkomstmaat. De multipele lineaire regressieanalyse (tabel 3) toont dat de primaire uitkomst, het verschil tussen de gemiddelde serumcreatinineconcentratie en die bij aanvang, onafhankelijk was van CCAB-behandeling (β = −0,023; 95%-betrouwbaarheidsinterval [95%-BI] = −12,2-7,2; P = 0,615).
Propensity score matching resulteerde in 134 paren met CCAB behandelde en niet-behandelde patiënten (tabel 4). De patiëntkarakteristieken laten geen verschil tussen beide groepen zien. Matching resulteerde in twee identieke groepen. De propensity score was samen met de cumulatieve CCAB-dosering als onafhankelijke variabele opgenomen in een multipele lineair regressiemodel (tabel 5). De cumulatieve CCAB-dosering bleek niet gerelateerd aan de primaire uitkomstmaat (β = 0,299; 95%-BI = −0,38-0,98; P = 0,388). Hetzelfde resultaat werd verkregen als CCAB-behandeling als binaire variabele werd ingevoegd in plaats van de cumulatieve CCAB-dosis.
Secundaire uitkomstmaten
De secundaire uitkomsten renale SOFA-score, RIFLE-score en CVVHD lieten geen significante verschillen zien tussen beide cohorten (tabel 2).
Beschouwing
Dit onderzoek laat zien dat CCAB met TDM geen nefrotoxiciteit veroorzaakt bij IC-patiënten. Deze bevinding weerlegt de opvatting dat alle toedieningswijzen van conventioneel amfotericine B nefrotoxisch zijn.
Dit is de eerste studie die aantoont dat CCAB niet nefrotoxisch is als preventieve antischimmeltherapie bij IC-patiënten met abdominale sepsis, waarbij CCAB een groot economisch voordeel biedt ten opzichte van andere antischimmelmiddelen [2,19]. Bovendien zijn er geen studies die superioriteit in effectiviteit of mortaliteit aantonen van andere antifungale behandelingen ten opzichte van CCAB [1,2,18,25,26].
Onze resultaten zijn in overeenstemming met andere onderzoeken, waaruit bleek dat de nierfunctiestoornis mild en reversibel was na behandeling met CCAB [2,18-20,25,27]. Door CCAB worden hoge topspiegels vermeden die kunnen resulteren in nefrotoxiciteit [18-20]. In tegenstelling tot CCAB wordt c-AmB als eenmaaldaagse infusie geassocieerd met aanzienlijke niertoxiciteit [9,10,13-17]. Dit heeft mede geleid tot de ontwikkeling en toepassing van nieuwe, duurdere antischimmelmiddelen, waaronder lipidenformuleringen van amfotericine B, breedspectrumazolen en echinocandinen. Deze nieuwe antifungale middelen zijn niet met CCAB vergeleken, enkel met c-AmB [1,11,12,28,29].
TDM kan hebben bijgedragen aan het verkrijgen van effectieve serumwaarden en tegelijkertijd aan het voorkomen van nefrotoxiciteit [2]. Referentiewaarden voor TDM van amfotericine B zijn gebaseerd op het bereiken van fungicide intra-abdominale concentraties [5]. Toediening van c-AmB als eenmaaldaagse infusie resulteert in hogere serumconcentraties in vergelijking met toediening van CCAB. Dit resulteert in grotere en snellere distributie in de nieren wat nefrotoxiciteit kan veroorzaken [2,30]. Het effect van amfotericine B lijkt concentratie- en tijdsafhankelijk, waardoor de kans op nefrotoxiciteit bij CCAB vergeleken tot c-AmB lager is [2].
Onze resultaten tonen voor geen van alle uitkomstmaten voor nefrotoxiciteit een relatie met CCAB. Daarbij werden voor het primaire eindpunt, serumcreatinineconcentratie over tijd, meerdere analyses uitgevoerd, namelijk propensity score matching, univariate en multipele lineaire regressie. Bovendien bevatten de eindpunten alle dagelijks gemeten laboratoriumwaarden tijdens IC-opname, terwijl andere studies alleen de hoogste waarde tijdens behandeling rapporteerden. Hierdoor werden potentiële niet door CCAB veroorzaakte uitschieters vermeden.
De retrospectieve niet-gerandomiseerde opzet van deze studie vereist voorzichtigheid bij de interpretatie van de bevinding, omdat deze opzet kan leiden tot selectiebias. De selectiebias voor mogelijk ziekere patiënten door intensivisten in OLVG en het lagere serumcreatinine bij aanvang in de CCAB-groep kunnen zorgen voor een nadelig effect voor CCAB wat betreft nefrotoxiciteit.
De mogelijke selectiebias is ingeperkt door vergelijkbare cohorten te creëren middels regressie en propensity score matching. Een andere beperking is de specifieke indicatie waarvoor in beide centra CCAB wordt toegepast. Voorzichtigheid is geboden bij het extrapoleren van onze resultaten naar andere indicaties.
Conclusie
Deze studie toont aan dat CCAB met TDM geen nefrotoxiciteit veroorzaakt bij IC-patiënten.
Verantwoording
Geen belangenverstrengeling gemeld.
Literatuur
1. Johansen HK, Gøtzsche PC. Amphotericin B lipid soluble formulations versus amphotericin B in cancer patients with neutropenia. Cochrane Database Syst Rev. 2014 Sep 4;2014(9):CD000969.
2. Falci DR, dos Santos RP, Wirth F, Goldani LZ. Continuous infusion of amphotericin B deoxycholate: an innovative, low-cost strategy in antifungal treatment. Mycoses. 2011 Mar;54(2):91-8.
3. Eggimann P, Bille J, Marchetti O. Diagnosis of invasive candidiasis in the ICU. Ann Intensive Care. 2011 Sep 1;1:37.
4. van de Veerdonk FL, Kolwijck E, Lestrade PP, et al. Influenza-Associated Aspergillosis in Critically Ill Patients. Am J Resp Crit Care Med. 2017 Aug 15;196(4):524-527.
5. van der Voort PH, Boerma EC, Yska JP. Serum and intraperitoneal levels of amphotericin B and flucytosine during intravenous treatment of critically ill patients with Candida peritonitis. J Antimicrob Chemother. 2007 May;59(5):952-6.
6. Parkins MD, Sabuda DM, Elsayed S, Laupland KB. Adequacy of empirical antifungal therapy and effect on outcome among patients with invasive Candida species infections. J Antimicrob Chemother. 2007 Sep;60(3):613-8.
7. Poissy J, Damonti L, Bignon A, et al. Risk factors for candidemia: a prospective matched case-control study. Crit Care. 2020 Mar 18;24(1):109.
8. Bassetti M, Giacobbe DR, Vena A, et al. Incidence and outcome of invasive candidiasis in intensive care units (ICUs) in Europe: results of the EUCANDICU project. Crit Care. 2019 Jun 14;23(1):219.
9. Peleg AY, Woods ML. Continuous and 4 h infusion of amphotericin B: a comparative study involving high-risk haematology patients. J Antimicrob Chemother. 2004 Oct;54(4):803-8.
10. Maharom P, Thamlikitkul V. Implementation of clinical practice policy on the continuous intravenous administration of amphotericin B deoxycholate. J Med Assoc Thai. 2006 Nov;89 Suppl 5:S118-24.
11. Kullberg BJ, Sobel JD, Ruhnke M, et al. Voriconazole versus a regimen of amphotericin B followed by fluconazole for candidaemia in non-neutropenic patients: a randomised non-inferiority trial. Lancet. 2005 Oct 22-28;366(9495):1435-42.
12. Walsh TJ, Finberg RW, Arndt C, et al. Liposomal amphotericin B for empirical therapy in patients with persistent fever and neutropenia. National Institute of Allergy and Infectious Diseases Mycoses Study Group. N England J Med. 1999 Mar 11;340(10):764-71.
13. Tissot F, Agrawal S, Pagano L, et al. ECIL-6 guidelines for the treatment of invasive candidiasis, aspergillosis and mucormycosis in leukemia and hematopoietic stem cell transplant patients. Haematologica. 2017 Mar;102(3):433-444.
14. Guery BP, Arendrup MC, Auzinger G, et al. Management of invasive candidiasis and candidemia in adult non-neutropenic intensive care unit patients: Part II. Treatment. Intensive Care Med. 2009 Feb;35(2):206-14.
15. Pappas PG, Kauffman CA, Andes DR, et al. Clinical Practice Guideline for the Management of Candidiasis: 2016 Update by the Infectious Diseases Society of America. Clin Infec Dis. 2016 Feb;62(4):e1-50.
16. Ullmann AJ, Aguado JM, Arikan-Akdagli S, et al. Diagnosis and management of Aspergillus diseases: executive summary of the 2017 ESCMID-ECMM-ERS guideline. Clin Microbiol Infect. 2018 May;24 Suppl 1:e1-e38.
17. Stichting Werkgroep Antibioticabeleid. SWAB Guidelines for the Management of Invasive Fungal Infections [internet]. Revised version released; 2017 dec 14 [geraadpleegd op 18/12/2020]. https://adult.swabid.nl/sites/default/files/SWAB%20Richtlijn%20Mycosen%202017%20%28final%29_compressed.pdf
18. Falagas ME, Karageorgopoulos DE, Tansarli GS. continuous versus conventional infusion of amphotericin B deoxycholate: a meta-analysis. PloS One. 2013 Oct;8(10):e77075.
19. Rothenbuhler C, Held U, Manz MG, Schanz U, Gerber B. Continuously infused amphotericin B deoxycholate for primary treatment of invasive fungal disease in acute myeloid leukaemia. Hematol Oncol. 2018 Apr;36(2):471-480.
20. Eriksson U, Seifert B, Schaffner A. Comparison of effects of amphotericin B deoxycholate infused over 4 or 24 hours: randomised controlled trial. BMJ. 2001 Mar 10;322(7286):579-82.
21. Nivoix Y, Ledoux MP, Herbrecht R. Antifungal Therapy: New and Evolving Therapies. Semin Respiratory Crit Care Med. 2020 Feb;41(1):158-174.
22. Bellomo R, Ronco C, Kellum JA, Mehta RL, Palevsky P. Acute renal failure - definition, outcome measures, animal models, fluid therapy and information technology needs: the Second International Consensus Conference of the Acute Dialysis Quality Initiative (ADQI) Group. Crit Care. 2004 Aug;8(4):R204-12.
23. Rosenbaum PR, Rubin DB. The Central Role of the Propensity Score in Observational Studies for Causal Effects. Biometrika. 1983 Apr;70(1):41-55.
24. Groenwold RH. [Propensity scores in observational research]. Ned Tijdschr Geneeskd. 2013;157(29):A6179.
25. Dreyfuss D, Ricard JD, Gaudry S. Amphotericin B deoxycholate for candidiasis in intensive care unit patients revisited: medical, ethical, and financial implications. Am J Respir Crit Care Med. 2013 Mar 15;187(6):661-3.
26. Johnson PC, Wheat LJ, Cloud GA, et al. Safety and efficacy of liposomal amphotericin B compared with conventional amphotericin B for induction therapy of histoplasmosis in patients with AIDS. Ann Intern Med. 2002 Jul 16;137(2):105-9.
27. Gwee A, Cranswick N, Connell TG, Curtis N. Minimizing nephrotoxicity using continuous infusion of deoxycholate amphotericin B. Pediatr Infect Dis J. 2014 Oct;33(10):1098.
28. Prentice HG, Hann IM, Herbrecht R, et al. A randomized comparison of liposomal versus conventional amphotericin B for the treatment of pyrexia of unknown origin in neutropenic patients. Br J Haematol. 1997 Sep;98(3):711-8.
29. Mora-Duarte J, Betts R, Rotstein C, et al. Comparison of caspofungin and amphotericin B for invasive candidiasis. N Engl J Med. 2002 Dec 19;347(25):2020-9.
30. Lewis RE, Wiederhold NP. The solubility ceiling: a rationale for continuous infusion amphotericin B therapy? Clin Infect Dis. 2003 Sep 15;37(6):871-2.
Referentie
Citeer als: Geersing TH, van der Voort PHJ, Spronk PE, van Kan HJM, den Reijer PM, Franssen EJF. Geen nefrotoxiciteit na continue infusie amfotericine B met TDM bij ernstig zieke patiënten met abdominale sepsis. Nederlands Platform voor Farmaceutisch Onderzoek. 2021;6:a1746.
DOI
https://www.knmp.nl/resolveuid/42111d1b4b404aed9d4b736d0a2f8a1dOpen access






Reactie toevoegen