Gebruik van een vaste dosering voor monoklonale antilichamen binnen de oncologie
- Rubriek: Overzichtsartikel
- Identificatie: 2018;3:a1677
Kernpunten
- Vanwege het farmacokinetische gedrag van monoklonale antilichamen is het mogelijk om een vaste dosering te geven in plaats van een dosering op basis van lichaamsgrootte.
- Variabiliteit in blootstelling tussen patiënten bij monoklonale antilichamen is kleiner bij het gebruik van een vaste dosering dan bij doseren op basis van lichaamsgewicht.
- Het doseren van monoklonale antilichamen in een vaste dosering leidt tot betere veiligheid bij het voor toediening gereed maken en tot minder spillage.
Abstract
Fixed dosing of monoclonal antibodies in oncology
BACKGROUND and OBJECTIVE
Most monoclonal antibodies in oncology are administered using body size-based dosing schedules. This is believed to correct for variability in both drug distribution and elimination between patients. However, the minor effects of body size on distribution and elimination of monoclonal antibodies and their usually wide therapeutic window do not support body size-based dosing.
DESIGN and METHODS
We summarized effects of body weight on the pharmacokinetic parameters of monoclonal antibodies in oncology and show that a fixed dose for most of these drugs is justified.
RESULTS and CONCLUSION
We show that fixed dosing is justified and can improve efficiency of compounding. Moreover, drug spillage can be reduced and medication errors may become less likely.
Inleiding
Binnen de oncologie worden de meeste intraveneus toegediende geneesmiddelen niet in een vaste dosering gegeven, maar gedoseerd op basis van lichaamsoppervlakte of lichaamsgewicht. De oorsprong hiervan ligt in het smalle therapeutische venster van chemotherapie [1]. Onderzoek uit de periode 1950-1970 laat zien dat de maximaal tolereerbare doseringen (MTDs) van cytotoxische middelen bij proefdieren overeen kwamen met de MTDs bij mensen, indien de doseringen werden geschaald op basis van lichaamsoppervlakte [2,3]. Hierdoor werd het mogelijk om voor nieuwe cytostatica betere startdoseringen voor fase I-studies te bepalen op basis van de preklinische data [1]. Het doseren op basis van lichaamsoppervlakte werd vervolgens ook gebruikt bij de behandeling van patiënten om te corrigeren voor variatie tussen individuen in farmacokinetische parameters, zoals verdeling van geneesmiddelen over het lichaam en eliminatieprocessen [1,4].
Bij de introductie van monoklonale antilichamen binnen de oncologie zijn de doseringen van deze monoklonale antilichamen ook gebaseerd op het lichaamsoppervlakte of lichaamsgewicht van patiënten. Rituximab werd in klinische studies onderzocht in doseringen van 375 tot 500 mg/m2 en is in 1998 ook geregistreerd op basis van een dosering op lichaamsoppervlakte voor de behandeling van non-Hodgkin lymfoom [5]. Bij de ontwikkeling van trastuzumab voor de behandeling van HER2-positieve borstkanker werd initieel 100 mg gebruikt als dosering in klinische studies [6,7]. Later is de dosering van trastuzumab op basis van ongepubliceerde fase I-studies gewijzigd naar een dosering op basis van lichaamsgewicht en is deze dosering ook de geregistreerde dosering geworden [8]. Tegenwoordig worden binnen de oncologie geregistreerde monoklonale antilichamen voornamelijk gedoseerd op basis van lichaamsgewicht (tabel 1) [9].
Recent hebben wij een literatuuronderzoek uitgevoerd, waarin vastgesteld werd dat monoklonale antilichamen veilig en effectief in een vaste dosering kunnen worden gegeven [9]. Dit artikel is vrij toegankelijk via de website van The Oncologist. De aanleiding voor beoordeling van de literatuur was de wens om de efficiëntie van het voor toediening gereedmaken (VTGM) van monoklonale antilichamen te verhogen door gebruik te maken van een vaste dosering per middel. Daarnaast kan een vaste dosering bijdragen aan het voorkòmen van medicatiefouten en het verminderen van spillage bij het VTGM-proces als gevolg van restanten in de flacons. In dit artikel zullen wij de bevindingen uit de oorspronkelijke publicatie bespreken. In het oorspronkelijke artikel is een overzicht opgenomen van alle geregistreerde monoklonale antilichamen binnen de oncologie [9]. In dit overzicht is voor elk van de middelen een voorstel gedaan voor een vaste dosering. Dit overzicht is bijgewerkt naar aanleiding van recente publicaties (tabel 1). Tevens hebben we in dit artikel de implementatie van een vaste dosering van monoklonale antilichamen binnen het Antoni van Leeuwenhoek beschreven zodat onze ervaring gebruikt kan worden bij implementatie in andere ziekenhuizen.
Farmacokinetiek van monoklonale antilichamen
Het farmacokinetisch gedrag van monoklonale antilichamen is complex en verschilt sterk van kleine moleculen [10]. Voor een verdieping in de farmacokinetiek van monoklonale antilichamen wordt verwezen naar het addendum dat geldt als een achtergrondoverzicht bij dit artikel. De verdeling van monoklonale antilichamen over het lichaam beperkt zich door hun grootte en hydrofiliciteit tot de bloedbaan en het extracellulaire vocht, wat zich vertaalt in een klein distributievolume (meestal 2 tot 12 liter) [10,11]. Monoklonale antilichamen worden niet hepatisch of renaal geklaard, maar afgebroken tot peptiden en aminozuren via een non-specifieke afbraakroute voor IgG (proteolytisch katabolisme) en een specifieke afbraakroute via binding aan het doelwit (figuur 1 en tabel 2) [10,11]. Bij therapeutische bloedspiegels is de trage, lineaire niet-specifieke afbraakroute de snelheidsbepalende stap en daardoor ontstaat de lange eliminatiehalfwaardetijd van monoklonale antilichamen.
Effecten van lichaamsgewicht op farmacokinetiek monoklonale antilichamen
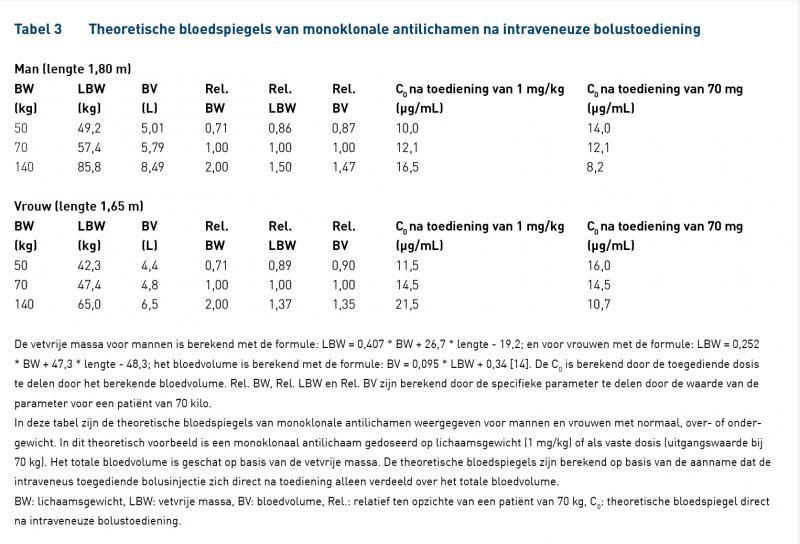
Omdat monoklonale antilichamen zich alleen over de bloedbaan en het extracellulaire vocht verdelen is de invloed van het lichaamsgewicht op het verdelingsvolume beperkt [12,13]. Hoewel het bloedvolume ten opzichte van patiënten met een normaal gewicht toeneemt in patiënten met overgewicht en afneemt in patiënten met ondergewicht, is de verandering in bloedvolume sterk minder dan proportioneel met de verandering in lichaamsgewicht [14,15]. Hierdoor zal een lineair doseringsschema voor monoklonale antilichamen (bijvoorbeeld op basis van mg/kg) leiden tot hogere bloedspiegels in patiënten met overgewicht, en tot lagere bloedspiegels in patiënten met ondergewicht (tabel 3).
Zoals hiervoor beschreven worden monoklonale antilichamen via twee routes afgebroken: door proteolytisch katabolisme en door intracellulaire afbraak na binding aan het doelwit. De intracellulaire afbraak van het antilichaam-doelwitcomplex is uiteraard niet afhankelijk van het lichaamsgewicht, maar voornamelijk afhankelijk van tumorvolume, affiniteit van het monoklonale antilichaam voor het doelwit en mate van expressie van het doelwit in de tumoren ten opzichte van endogene expressie [9]. Afbraak via proteolytisch katabolisme is wel lichaamsgewicht afhankelijk doordat de afbraak plaatsvindt in de endosomale ruimte, welke geschat wordt op 0,5% van het totale weefselvolume [16]. De klinische relevantie hiervan is echter beperkt aangezien de absolute eliminatie via proteolytisch katabolisme beperkt is en de relatie tussen het lichaamsgewicht en de endosomale ruimte zwak is.
Doseren op lichaamsgewicht versus vaste doseringen
Hoewel de farmacokinetiek van monoklonale antilichamen anders is in patiënten met over- en ondergewicht dan patiënten met een normaal gewicht, is de verandering in farmacokinetiek kleiner dan de verandering in lichaamsgewicht (tabel 3). Dit zorgt ervoor dat patiënten met ondergewicht een relatief lage dosering krijgen ten opzichte van patiënten met een normaal gewicht en patiënten met overgewicht een relatief hoge dosering krijgen als er op lichaamsgewicht gedoseerd wordt. Bij een vaste dosering is dit logischerwijs omgekeerd. Hieruit ontstaat de vraag of een vaste dosering leidt tot meer, evenveel of minder variabiliteit in de populatie dan een dosering op basis van lichaamsgewicht. Voor een patiënt met een gemiddeld gewicht maakt het doseerschema niet uit omdat de vaste dosering vaak gebaseerd is op patiënten met een gemiddeld gewicht. In een farmacologische simulatiestudie hebben Wang et al. een dosering op lichaamsgewicht vergeleken met een vaste dosering [17]. In dit model is een mediaan lichaamsgewicht van 75,5 kg (bereik 38,8 – 187,2 kg) gebruikt om de oppervlakte onder de plasmaconcentratie-tijdcurve (AUC) te schatten na een vaste dosering en een dosering op lichaamsgewicht. In populatiemodellen worden het verdelingsvolume en de klaring in de populatie meestal gecorrigeerd voor het individuele gewicht door de parameter te vermenigvuldigen met de volgende vergelijking:
In deze vergelijking staat BW voor bodyweight, het lichaamsgewicht en BWm voor mean bodyweight, het gemiddelde lichaamsgewicht van de populatie. De exponent (exp) wordt gebruikt om het effect van het lichaamsgewicht weer te geven, waarbij 0 staat voor geen effect en 1 staat voor een lineair effect. Deze exponent wordt geschat in het farmacokinetisch populatiemodel bij het beschrijven van data verkregen uit klinische studies. Uit de simulatiestudie van Wang et al. bleek dat, wanneer een exponent < 0,32 werd gevonden als exponent in formule 1 om te corrigeren voor verschil in klaring, een vaste dosering leidt tot minder dan 20% variatie in AUC tussen patiënten met overgewicht en patiënten met normaal gewicht [17]. Voor een dosering gebaseerd op lichaamsgewicht werd minder dan 20% variatie in AUC gevonden als de exponent > 0,68 bedraagt. Beide doseerstrategieën resulteerden in maximaal 100% variatie in AUC ten opzichte van een normaal gewicht. Deze resultaten zijn bevestigd door Bai et al., waarbij ook werd aangetoond dat een vaste dosering leidt tot minder variabiliteit in AUC dan een dosering gebaseerd op lichaamsgewicht indien deze exponent < 0,5 is [18]. Een vaste dosering leidde bij deze exponent ook tot minder variabiliteit in maximale plasmaconcentraties (Cmax). Samengevat laten deze data zien dat een vaste dosering minder variabiliteit geeft dan een dosering gebaseerd op lichaamsgewicht als deze toegepast wordt bij monoklonale antilichamen met een beperkt effect (een gebruikte exponent < 0,5 in populatiemodellen) van lichaamsgewicht op verdelingsvolume en klaring.
Rechtvaardiging vaste doseringen monoklonale antilichamen binnen de oncologie
Het effect van lichaamsgewicht op het verdelingsvolume en de klaring van monoklonale antilichamen staat vaak vermeld in de wetenschappelijke discussie die onderdeel is van de openbare beoordelingsrapporten van de Europese registratieautoriteit (EMA). Deze gegevens zijn echter vaak gebaseerd op beperkte data van fase I- en II-studies. Meer informatie kan vaak worden gewonnen uit publicaties die, bijvoorbeeld, populatiemodellen beschrijven. In tabel 1 hebben we de effecten van lichaamsgewicht op distributievolume en klaring samengevat van monoklonale antilichamen die binnen de oncologie worden gebruikt. Van de 16 monoklonale antilichamen die binnen de oncologie gebruikt worden zijn er vijf geregistreerd met een vaste dosering (atezolizumab, catumaxomab, obinutuzumab, ofatumumab en pertuzumab). In 2016 heeft de Amerikaanse registratieautoriteit (FDA) de geregistreerde dosering voor nivolumab aangepast[19]. De oorspronkelijke geregistreerde dosering (3 mg/kg) is omgezet naar een vaste dosering van 240 mg voor alle patiënten. Deze aanpassing is gebaseerd op populatiemodellen en dosis-responsevaluaties. De FDA kwam tot de conclusie dat de blootstelling in beide doseerregimes vergelijkbaar was en dat de dosis-responscurve relatief vlak was.
Zoals hiervoor beschreven zorgt een vaste dosering voor minder variabiliteit als beperkte effecten (een gebruikte exponent < 0,5 in populatiemodellen) van het lichaamsgewicht op verdelingsvolume en lichaamsgewicht worden gezien. Daarom raden wij een vaste dosering aan voor cetuximab en bevacizumab, omdat er minimale effecten gezien zijn van lichaamsgewicht op deze farmacokinetische parameters en daarom de vaste dosering minder variabiliteit geeft dan de geregistreerde dosering op lichaamsgewicht [20-25].
Als er sterke effecten van het lichaamsgewicht op het verdelingsvolume en de klaring gezien worden (een gebruikte exponent > 0,68 in populatiemodellen), zorgt een dosering op lichaamsgewicht voor minder variabiliteit dan een vaste dosering [17]. Omdat monoklonale antilichamen vaak een grote therapeutische breedte hebben, kan een vaste dosering nog steeds om praktische redenen overwogen worden. De maximale variabiliteit in AUC die verwacht kan worden ten opzichte van de gemiddelde AUC van de geregistreerde dosering bedraagt ~ 100% [17]. De meeste monoklonale antilichamen binnen de oncologie hebben een dusdanige therapeutische breedte dat een variabiliteit van 100% geen belemmering vormt voor een vaste dosering. In tabel 1 hebben wij voor elk middel een vaste dosering vastgesteld. Voor de gedetailleerde onderbouwing van deze vaste dosering wordt verwezen naar het addendum bij dit artikel.
Hoewel voor de meeste monoklonale antilichamen binnen de oncologie een vaste dosering voor alle patiënten gerechtvaardigd is, zijn er enkele monoklonale antilichamen waarbij een vaste dosering alleen gerechtvaardigd is indien er meerdere doseringen gebruikt worden, elk voor een bepaalde gewichtscategorie (dose banding).
Ipilimumab, een monoklonaal antilichaam gericht tegen CTLA-4, laat een dosis-repons en een dosis-toxiciteitrelatie zien die grotendeels overlappen [26,27]. Een dosering van 10 mg/kg ipilimumab is tolereerbaar na herhaaldelijke toediening en beperkt effectiever dan een dosering van 3 mg/kg, maar zorgt tevens voor meer ernstige, dosislimiterende bijwerkingen. Een kwart van de patiënten moet voortijdig staken met de behandeling bij deze dosering. Anderzijds laat een dosering van 0,1 mg/kg een verminderde effectiviteit zien. Behandeling met een dosering van 0,1 mg/kg is hiermee niet gerechtvaardigd. Zoals in tabel 1 is beschreven, kunnen er voor ipilimumab drie gewichtscategorieën aangemerkt worden waarbij een vaste dosering kan worden gebruikt die gebaseerd is op de beschikbare flaconsterktes. Zo krijgen bijvoorbeeld alle patiënten tussen de 60 en 100 kg een vaste dosering van 250 mg. Dit resulteert in een individuele dosering van 2,5-4,2 mg/kg (geregistreerde aanbevolen dosering is 3 mg/kg).
Panitumumab is een monoklonaal antilichaam met de epidermale groeifactorreceptor als doelwit. De effecten van het lichaamsgewicht op de farmacokinetiek van panitumumab zijn beperkt [26]. Voor panitumumab is echter beschreven dat de AUC niet lineair toeneemt bij doseringen tot 2 mg/kg en vanaf 2 mg/kg proportioneel toeneemt [27]. Dit impliceert dat vanaf een dosering van ~ 2 mg/kg volledige receptorbezetting plaatsvindt. Een minimale dosering van ~ 2 mg/kg per week zal daarom nodig zijn. Een vaste dosering voor verschillende gewichtscategorieën is daarom aan te raden (tabel 1).
Uit het populatiemodel van ramucirumab, een remmer van de vasculaire endotheliale groeifactor, is gebleken dat het effect van lichaamsgewicht op het verdelingsvolume en de klaring minimaal is (een exponent van respectievelijk 0,556 en 0,499)[28]. Recent is gekeken naar de dosis-effectiviteit- en dosis-toxiciteitrelatie van ramucirumab [29]. Hieruit bleek dat patiënten met een lage blootstelling een slechtere overleving lieten zien dan patiënten met een hoge blootstelling. Er bleek geen dosis-toxiciteitrelatie uit de analyse. Op basis van de effectiviteits- en toxiciteitsgegevens kan geconcludeerd worden dat de therapeutische breedte voldoende is voor de toepassing van een vaste dosering, maar dat het noodzakelijk is om patiënten tussen de 100 en 140 kg een hogere dosering te geven dan patiënten tussen de 60 en 100 kg om boven de gevonden minimale blootstelling te blijven.
Implementatie en kostenbesparing van vaste doseringen in de praktijk
Bij de introductie van ipilimumab voor de behandeling van gemetastaseerd melanoom in het Antoni van Leeuwenhoek is gekeken naar een veilige en efficiënte toepassing van dit dure middel (circa € 18.000 per gift). Door gebruik te maken van een vaste dosering werden voorschrijffouten en spillage geminimaliseerd. Na overleg tussen de voorschrijvende internist-oncologen en de ziekenhuisapothekers is besloten gebruik te maken van een dosering welke werd afgerond op hele flacons (50 mg). Toen meer data beschikbaar kwamen, is overgestapt naar een vaste dosering voor alle patiënten tussen de 60 en 100 kg. Bij de introductie van de PD-1-bindende antilichamen nivolumab en pembrolizumab is ook voor deze middelen direct een vaste dosering vastgesteld voor zowel de behandeling van melanomen als niet-kleincellig longcarcinoom binnen het Antoni van Leeuwenhoek. We hebben een analyse gemaakt van de impact van een vaste dosering op de kosten. Hiervoor hebben we een overzicht gemaakt van alle infusen met ipilimumab, nivolumab of pembrolizumab die binnen ons ziekenhuis zijn klaargemaakt (tabel 4). We hebben per infuus bekeken hoeveel flacons nodig zouden zijn geweest als er op basis van lichaamsgewicht zou zijn gedoseerd en hoeveel flacons er nodig waren voor de vaste dosering. Zo zouden er voor een patiënt van 90 kilogram bijvoorbeeld twee flacons van 100 mg en één flacon van 40 mg nodig zijn voor een nivolumab infuus van 240 mg. Op basis van de geregistreerde dosering zouden twee flacons van 100 mg en twee flacons van 40 mg nodig zijn geweest. Dit levert een besparing op van 1 flacon van 40 mg. Op deze manier hebben we een berekende besparing van meer dan € 3 miljoen gerealiseerd (tabel 4). Dit laat zien dat het gebruik van een vaste dosering kostenbesparend kan werken.
Na voltooien van de oorspronkelijke publicatie zijn alle, reeds binnen het Antoni van Leeuwenhoek in gebruik zijnde, monoklonale antilichamen geëvalueerd [9]. De rationale voor een vaste dosering is op basis van dit artikel gepresenteerd aan de internist-oncologen en tijdens de bijeenkomst is een door de ziekenhuisapotheek vastgestelde vaste dosering voorgesteld voor de twee meest voorgeschreven monoklonale antilichamen binnen het Antoni van Leeuwenhoek (bevacizumab en trastuzumab). Naar aanleiding van deze discussie is besloten om het elektronisch voorschrijfsysteem dusdanig in te richten dat alleen nog maar een vaste dosering voorgeschreven kon worden voor nieuwe patiënten. Patiënten die reeds een van deze middelen gebruikten konden overgezet worden op een vaste dosering of doorgaan op de oude dosering. De keuze werd door de behandelend arts in overleg met de patiënt gemaakt. Patiënten zijn door de behandelend artsen mondeling en schriftelijk geïnformeerd over het gebruik van de vaste doseringen. In navolging van bevacizumab en trastuzumab is recent voor de overige monoklonale antilichamen ook een vaste dosering voorgesteld, welke nu grotendeels geïmplementeerd zijn. Bij de introducties van nieuwe monoklonale antilichamen binnen het ziekenhuis worden sinds augustus 2017 standaard de dosis-effectiviteitsrelatie en de dosis-toxiciteitsrelatie door de ziekenhuisapotheek geëvalueerd en volgt een voorstel voor de vaste dosering richting de internist-oncologen. Hiermee zijn in het Antoni van Leeuwenhoek stappen gezet om binnen afzienbare tijd alle monoklonale antilichamen te doseren in een vaste dosering. Hiermee wordt de efficiëntie bij het maken van de infusen vergroot en een forse kostenbesparing gerealiseerd.
Conclusie
Uit openbare beoordelingsrapporten van het EMA en uit gepubliceerde literatuur blijkt dat voor de meeste monoklonale antilichamen geldt dat het lichaamsgewicht een matig tot beperkt effect heeft op de farmacokinetische parameters [9]. Daar staat tegenover dat voor monoklonale antilichamen geldt dat er een minimale bloedspiegel nodig is om nagenoeg volledige bezetting van het doelwit te bewerkstelligen en dat boven deze grenswaarde geen effect gezien wordt tussen dosis en effectiviteit of tussen dosis en toxiciteit [9]. Doordat monoklonale antilichamen een groot therapeutisch venster hebben, kan op basis van praktische redenen een vaste dosering gegeven worden in plaats van te doseren op lichaamsgewicht.
Met dit artikel tonen wij aan dat het voor monoklonale antilichamen binnen de oncologie mogelijk is om een vaste dosering te geven, zonder dat de middelen minder effectief of toxischer worden. Bovendien kan dit leiden tot een aanzienlijke kostenbesparing. Wij zijn daarom van mening dat een vaste dosering van monoklonale antilichamen gebaseerd kan worden op resultaten uit populatiemodellen en registratieonderzoeken. De vaste dosering kan de medicatieveiligheid vergroten en helpen om een besparing in de zorgkosten te realiseren zonder dat de effectiviteit of de veiligheid van deze middelen in het geding komt.
Downloads
Verantwoording
Geen belangenverstrengeling gemeld.
Dit artikel is een bewerkte vertaling van: Hendrikx JJMA, Haanen JBAG, Voest EE, Schellens JHM, Huitema ADR, Beijnen JH. Fixed dosing of monoclonal antibodies in oncology. The Oncologist. 2017;22:1212-1221. In dit Nederlandstalige artikel zijn relevante gegevens toegevoegd uit literatuur die beschikbaar is gekomen na publicatie van het oorspronkelijke artikel.
Literatuur
1. Sawyer M en MJ Ratain. Body surface area as a determinant of pharmacokinetics and drug dosing. Invest New Drugs. 2001;19:171-177.
2. Freireich EJ, EA Gehan, DP Rall, et al. Quantitative comparison of toxicity of anticancer agents in mouse, rat, hamster, dog, monkey, and man. Cancer ChemotherRep. 1966;50:219-244.
3. Pinkel. The use of body surface area as a criterion of drug dosage in cancer chemotherapy. Cancer Res. 1958;18:853-856.
4. Crawford JD, ME Terry,GM Rourke. Simplification of drug dosage calculation by application of the surface area principle. Pediatrics. 1950;5:783-790.
5. Grillo-Lopez AJ, CA White, C Varns, et al. Overview of the clinical development of rituximab: First monoclonal antibody approved for the treatment of lymphoma. SeminOncol. 1999;26:66-73.
6. Baselga J, D Tripathy, J Mendelsohn, et al. Phase ii study of weekly intravenous recombinant humanized anti-p185her2 monoclonal antibody in patients with her2/neu-overexpressing metastatic breast cancer. JClinOncol. 1996;14:737-744.
7. Pegram MD, A Lipton, DF Hayes, et al. Phase ii study of receptor-enhanced chemosensitivity using recombinant humanized anti-p185her2/neu monoclonal antibody plus cisplatin in patients with her2/neu-overexpressing metastatic breast cancer refractory to chemotherapy treatment. JClinOncol. 1998;16:2659-2671.
8. Tokuda Y, T Watanabe, Y Omuro, et al. Dose escalation and pharmacokinetic study of a humanized anti-her2 monoclonal antibody in patients with her2/neu-overexpressing metastatic breast cancer. Br J Cancer. 1999;81:1419-1425.
9. Hendrikx JJMA, JBAG Haanen, EE Voest, et al. Fixed dosing of monoclonal antibodies in oncology. The Oncologist. 2017;22:1212-1221.
10. Keizer RJ, AD Huitema, JH Schellens, et al. Clinical pharmacokinetics of therapeutic monoclonal antibodies. ClinPharmacokinet. 2010;49:493-507.
11. Mould DRand B Green. Pharmacokinetics and pharmacodynamics of monoclonal antibodies: Concepts and lessons for drug development. BioDrugs. 2010;24:23-39.
12. Bearden DTand KA Rodvold. Dosage adjustments for antibacterials in obese patients: Applying clinical pharmacokinetics. ClinPharmacokinet. 2000;38:415-426.
13. Hanley MJ, DR Abernethy,DJ Greenblatt. Effect of obesity on the pharmacokinetics of drugs in humans. ClinPharmacokinet. 2010;49:71-87.
14. Boer P. Estimated lean body mass as an index for normalization of body fluid volumes in humans. Am J Physiol. 1984;247:F632-F636.
15. Lemmens HJ, DP Bernstein,JB Brodsky. Estimating blood volume in obese and morbidly obese patients. Obes Surg. 2006;16:773-776.
16. Garg Aand JP Balthasar. Physiologically-based pharmacokinetic (pbpk) model to predict igg tissue kinetics in wild-type and fcrn-knockout mice. J Pharmacokinet Pharmacodyn. 2007;34:687-709.
17. Wang DD, S Zhang, H Zhao, et al. Fixed dosing versus body size-based dosing of monoclonal antibodies in adult clinical trials. J Clin Pharmacol. 2009;49:1012-1024.
18. Bai S, K Jorga, Y Xin, et al. A guide to rational dosing of monoclonal antibodies. Clin Pharmacokinet. 2012;51:119-135.
19. Modification of the dosage regimen for nivolumab. FDA announcement; 13 september 2016. Beschikbaar op: http://www.fda.gov/Drugs/InformationOnDrugs/ApprovedDrugs/ucm520871.htm [geraadpleegd op 26 januari 2018].
20. Avastin - epar scientific discussion. European Medicines Agency; 2006. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
21. Erbitux - epar scientific discussion. European Medicines Agency; 2006. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
22. Avastin - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
23. Erbitux - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
24. Azzopardi N, T Lecomte, D Ternant, et al. Cetuximab pharmacokinetics influences progression-free survival of metastatic colorectal cancer patients. Clin Cancer Res. 2011;17:6329-6337.
25. Lu JF, R Bruno, S Eppler, et al. Clinical pharmacokinetics of bevacizumab in patients with solid tumors. Cancer Chemother Pharmacol. 2008;62:779-786.
26. Ma P, BB Yang, YM Wang, et al. Population pharmacokinetic analysis of panitumumab in patients with advanced solid tumors. J Clin Pharmacol. 2009;49:1142-1156.
27. Ketzer S, K Schimmel, M Koopman, et al. Clinical pharmacokinetics and pharmacodynamics of the epidermal growth factor receptor inhibitor panitumumab in the treatment of colorectal cancer. Clinical Pharmacokinetics. 2017
28. O'Brien L, P Westwood, L Gao, et al. Population pharmacokinetic meta-analysis of ramucirumab in cancer patients. British Journal of Clinical Pharmacology. 2017;83:2741-2751.
29. Cohn AL, T Yoshino, V Heinemann, et al. Exposure-response relationship of ramucirumab in patients with advanced second-line colorectal cancer: exploratory analysis of the raise trial. Cancer Chemotherapy and Pharmacology. 2017;80:599-608.
30. Heery CR, G O'Sullivan-Coyne, RA Madan, et al. Avelumab for metastatic or locally advanced previously treated solid tumours (javelin solid tumor): A phase 1a, multicohort, dose-escalation trial. The Lancet Oncology. 2017;18:587-598.
31. Bavencio - epar scientific discussion. 2017. European Medicines Agency; 2017. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
32. Tecentriq - epar scientific discussion. European Medicines Agency; 2017. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
33. Removab - epar product information. European Medicines Agency; 2014. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
34. Removab - epar scientific discussion. European Medicines Agency; 2009. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
35. Feng Y, E Masson, D Dai, et al. Model-based clinical pharmacology profiling of ipilimumab in patients with advanced melanoma. Br J Clin Pharmacol. 2014;78:106-117.
36. Yervoy - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
37. Yervoy - epar scientific discussion. European Medicines Agency; 2011. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
38. Opdivo - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
39. Opdivo - epar scientific discussion. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
40. Gibiansky E, L Gibiansky, DJ Carlile, et al. Population pharmacokinetics of obinutuzumab (ga101) in chronic lymphocytic leukemia (cll) and non-hodgkin's lymphoma and exposure-response in cll. CPT Pharmacometrics Syst Pharmacol. 2014;3:e144.
41. Gazyvaro - epar scientific discussion. European Medicines Agency; 2014. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
42. Gazyvaro - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
43. Struemper H, M Sale, BR Patel, et al. Population pharmacokinetics of ofatumumab in patients with chronic lymphocytic leukemia, follicular lymphoma, and rheumatoid arthritis. J Clin Pharmacol. 2014;54:818-827.
44. Arzerra - epar scientific discussion. European Medicines Agency; 2010. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
45. Arzerra - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
46. Chiorean EG, C Sweeney, H Youssoufian, et al. A phase i study of olaratumab, an anti-platelet-derived growth factor receptor alpha (pdgfralpha) monoclonal antibody, in patients with advanced solid tumors. Cancer Chemotherapy and Pharmacology. 2014;73:595-604.
47. Mo G, JR Baldwin, D Luffer-Atlas, et al. Population pharmacokinetic modeling of olaratumab, an anti-pdgfralpha human monoclonal antibody, in patients with advanced and/or metastatic cancer. Clinical Pharmacokinetics. 2017
48. Lartruvo- epar scientific discussion. European Medicines Agency; 2017. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
49. Vectibix - epar scientific discussion. European Medicines Agency; 2007. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
50. Vectibix - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
51. Keytruda - epar scientific discussion. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
52. Keytruda - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
53. Ahamadi M, T Freshwater, M Prohn, et al. Model-based characterization of the pharmacokinetics of pembrolizumab: A humanized anti-pd-1 monoclonal antibody in advanced solid tumors. CPT Pharmacometrics Syst Pharmacol. 2017 Jan;6(1):49-57.
54. Ng CM, BL Lum, V Gimenez, et al. Rationale for fixed dosing of pertuzumab in cancer patients based on population pharmacokinetic analysis. Pharm Res. 2006;23:1275-1284.
55. Garg A, A Quartino, J Li, et al. Population pharmacokinetic and covariate analysis of pertuzumab, a her2-targeted monoclonal antibody, and evaluation of a fixed, non-weight-based dose in patients with a variety of solid tumors. Cancer Chemother Pharmacol. 2014;74:819-829.
56. Perjeta - epar scientific discussion. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
57. Perjeta - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
58. Cyramza - epar scientific discussion. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
59. Cyramza - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
60. Spratlin JL, RB Cohen, M Eadens, et al. Phase i pharmacologic and biologic study of ramucirumab (imc-1121b), a fully human immunoglobulin g1 monoclonal antibody targeting the vascular endothelial growth factor receptor-2. Journal of Clinical Oncology : official journal of the American Society of Clinical Oncology. 2010;28:780-787.
61. Ng CM, R Bruno, D Combs, et al. Population pharmacokinetics of rituximab (anti-cd20 monoclonal antibody) in rheumatoid arthritis patients during a phase ii clinical trial. J Clin Pharmacol. 2005;45:792-801.
62. Mabthera - epar scientific discussion. European Medicines Agency; 2006. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
63. Mabthera - epar product information. 2015. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
64. Bruno R, CB Washington, JF Lu, et al. Population pharmacokinetics of trastuzumab in patients with her2+ metastatic breast cancer. Cancer Chemother Pharmacol. 2005;56:361-369.
65. Cosson VF, VW Ng, M Lehle, et al. Population pharmacokinetics and exposure-response analyses of trastuzumab in patients with advanced gastric or gastroesophageal junction cancer. Cancer Chemother Pharmacol. 2014;73:737-747.
66. Herceptin - epar scientific discussion. European Medicines Agency; 2005. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
67. Herceptin - epar product information. European Medicines Agency; 2015. Beschikbaar op: http://www.ema.europa.eu [geraadpleegd op 26 januari 2018].
Referentie
Citeer als: Hendrikx JJMA, Haanen JBAG, Voest EE, Schellens JHM, Huitema ADR, Beijnen JH. Gebruik van een vaste dosering voor monoklonale antilichamen binnen de oncologie. Nederlands Platform voor Farmaceutisch Onderzoek. 2018;3:a1677.
DOI
https://www.knmp.nl/resolveuid/ff43b82f525d469aa3158a9c722ef4a4Open access






Reactie toevoegen