Hyperammoniëmische encefalopathie door valproïnezuur bij een patiënt op de geheugenpolikliniek
- Rubriek: Casuïstische mededeling
- Identificatie: 2021;6:a1736
Kernpunten
- Een valproïnezuurgemedieerde hyperammoniëmie komt naar schatting voor bij 35% van de gebruikers en verloopt vaak mild en asymptomatisch.
- Bij een klein deel van de gebruikers (< 2,5%) ontstaat echter encefalopathie met hoge morbiditeit.
- Bij een patiënt die zich presenteert met cognitieve en/of motorische achteruitgang – en zeker indien er ook traagheid of verandering in het bewustzijn is – dient valproïnezuurgebruik een alarmbel te zijn voor hyperammoniëmische encefalopathie.
Abstract
Hyperammonemic encephalopathy due to valproic acid in a patient visiting the memory clinic
Introduction
Hyperammonemia is not uncommon in patients receiving valproic acid. Few patients develop hyperammonemic encephalopathy but recognition of this side-effect is important since encephalopathy can present with a range of burdensome symptoms.
Description
A 57-year old male, with a history of brain injury and epilepsy after a motorcycle accident, was seen at our memory clinic with mental slowness, and initiative and memory loss. He was first diagnosed with cognitive impairment after brain injury and progression due to aging and stress. After a year, symptoms had worsened and also somnolence and balance disorders had developed. An elevated blood ammonia level of 174 μmol/L (reference = < 30 μmol/L) was found and attributed to valproic acid use. Valproic acid blood level was normal and there was no liver failure. Valproic acid was discontinued, the ammonia level normalized, and symptoms disappeared.
Discussion
Literature study shows that hyperammonemia is described in approximately 35% of valproic acid users. Hyperammonemia is mild and asymptomatic in most cases. The prevalence of hyperammonemic encephalopathy is low and varies from 0.1 to 2.5% of valproic acid users in large observational studies. Consciousness disturbance is an important symptom but encephalopathy can also present with cognitive, psychiatric, neuromotor and gastro-intestinal symptoms The exact mechanism of valproic acid-induced hyperammonemia is unclear but carnitine depletion seems to play an essential role. In patients with encephalopathy, valproic acid should be discontinued if possible. Other treatment options described in case-series include lactulose and levocarnitine.
Conclusion
In a patient presenting with cognitive and/or neuromotor symptoms, valproic acid use should raise suspicion for hyperammonemic encephalopathy.
Inleiding
Een 57-jarige man presenteerde zich op onze geheugenpolikliniek met traagheid, initiatiefverlies en geheugenproblemen. De klachten bleken uiteindelijk veroorzaakt te worden door hyperammoniëmische encefalopathie toegeschreven aan valproïnezuur.
In de literatuur worden hoge prevalentiecijfers van hyperammoniëmie bij valproïnezuur beschreven. Het ontwikkelen van encefalopathie is zeldzamer, maar het herkennen van deze bijwerking is belangrijk. In dit artikel willen wij u informeren over het vóórkomen, de verschillende symptomen en behandeling van valproïnezuurgemedieerde hyperammoniëmie.
Casusbeschrijving
Een man van 57 jaar, sinds 16-jarige leeftijd bekend met epilepsie door hersenletsel na een bromfietsongeval en bekend met hypercholesterolemie, werd gezien op de geheugenpolikliniek vanwege cognitieve achteruitgang. Zijn medicatielijst vermeldde valproïnezuur 4 dd 300 mg, oxcarbazepine 4 dd 600 mg, clobazam 1 dd 10 mg, simvastatine 1 dd 80 mg en ciprofibraat 1 dd 100 mg. Hij gebruikte de combinatie van anti-epileptica in deze doseringen al tenminste vier jaar.
Zijn leidinggevende van de sociale werkplaats en echtgenote was het opgevallen dat hij sinds enkele maanden steeds trager werd, weinig initiatief nam en geheugenproblemen had. Daarnaast noemde echtgenote dat er zorgen waren over haar ouders met dementie.
Tijdens een oriënterend psychiatrisch onderzoek waren er stoornissen in het kortetermijngeheugen en een vertraagd denktempo. De Mini Mental State Examination (MMSE)-score was 22/30 (score ≤ 24 is indicatief voor cognitieve stoornissen).
Ter uitsluiting van een directe anti-epileptica-intoxicatie werden de valproïnezuur-, oxcarbazepine- en clobazamspiegels bepaald, welke normaal waren. Een MRI van de hersenen liet een oud infarct rechts frontaal zien, geduid als gevolg van het bromfietsongeval. Er was geen opvallende atrofie of nieuwe vasculaire schade.
Bij neuropsychologisch onderzoek stond mentale traagheid op de voorgrond en werden een beperkte capaciteit van het werkgeheugen en stoornissen in de uitvoerende functies gevonden. Na multidisciplinair overleg werd de werkdiagnose ‘cognitieve stoornissen bij pre-existent hersenletsel met toename bij veroudering en stress’. Daarnaast werd gedacht aan een neurocognitief effect van langdurig anti-epilepticagebruik.
Bij controle een jaar later waren de klachten toegenomen. Patiënt bemerkte nu ook balansproblemen. Hij was voor onderzoek in het slaapcentrum geweest, omdat hij tijdens gesprekken in slaap viel. Een toxisch-medicamenteuze oorzaak werd opnieuw overwogen. Medicatiespiegels werden herhaald en ook ammoniak werd nu bepaald; arterieel ammoniak bleek fors verhoogd, 174 μmol/L (referentiewaarde laboratorium < 30 μmol/L). Medicatiespiegels waren opnieuw normaal. Er waren geen aanwijzingen voor leverfalen als verklaring voor de hyperammoniëmie; leverenzymen waren ≤ 1,5 maal de normaalwaarde en echografie van de lever toonde geen structurele afwijkingen.
Er werd gestart met lactulose en valproïnezuur werd door de behandelend neuroloog in zes maanden afgebouwd. Na zes maanden was het ammoniaklevel genormaliseerd (veneus = 37 μmol/L, referentiewaarde laboratorium 10 - 45 μmol/L) en werd lactulose gestopt. De klachten waren verdwenen (met nu een MMSE-score van 28/30) en bleven weg gedurende negen maanden follow-up.
Beschouwing
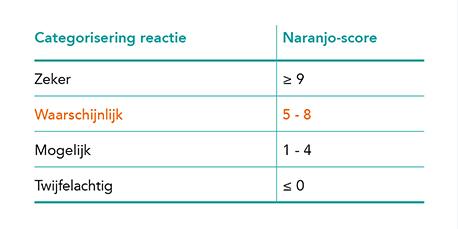
In deze casus werd hyperammoniëmie geconstateerd bij valproïnezuurgebruik. De Naranjo-score – voor het beoordelen van een oorzakelijk verband tussen geneesmiddel en bijwerking – is gescoord op een waarschijnlijk verband (tabel 1) [1].
Valproïnezuur is een frequent voorgeschreven anti-epilepticum en is ook geïndiceerd als stemmingsstabilisator. Het is bekend dat valproïnezuur hepatotoxisch kan zijn, maar ook zonder leverfalen kan leiden tot hyperammoniëmie [2]. Hoe hyperammoniëmie door valproïnezuur ontstaat is nog niet volledig opgehelderd. Het aminozuur carnitine speelt in ieder geval een rol. Valproïnezuur remt de synthese van carnitine, terwijl carnitine een belangrijke cofactor is in het transport van vetzuren als valproïnezuur over de mitochondriale membraan. Er vindt een verschuiving plaats in het metabolisme van valproïnezuur van bèta-oxidatie in de mitochondriën naar omega-oxidatie in het cytosol. Bij omega-oxidatie wordt een hogere valproïnezuurfractie omgezet in toxische metabolieten. De toxische metabolieten en valproïnezuur zelf zouden de productie van N-acetylglutamaat en het enzym carbamoylfosfaatsynthetase in de ureumcyclus remmen. Hierdoor wordt minder ammoniak omgezet in ureum [2].
Vóórkomen van hyperammoniëmie
Na overleg met Lareb bleek dat daar 22 meldingen van hyperammoniëmie in samenhang met valproïnezuur zijn binnengekomen. In VigiBase zijn 1476 meldingen opgenomen. De reporting odds ratio (ROR) is 245,3 en statistisch significant [3].
Chicharro et al. publiceerden in 2007 een review naar de prevalentie van hyperammoniëmie bij valproïnezuurgebruik en vonden gemiddelde prevalenties van 48 en 90%, gebaseerd op respectievelijk 14 cross-sectionele en 3 prospectieve studies [4].
In de PubMed-database werd gezocht naar studies die vanaf 2006 zijn verschenen – bij tenminste tien gebruikers van oraal valproïnezuur van 16 jaar of ouder – en niet zijn meegenomen in de genoemde review. Deze studies zijn weergegeven in tabel 2 [5-14].
De gemiddelde prevalentie vanuit vier prospectieve studies met in totaal 352 patiënten is 34,9% (spreiding = 25,4 - 55,3%) [5-8]. In zes retrospectieve studies varieert de gevonden frequentie sterk, van 11 - 83,3% (gemiddeld 43,5%, waarbij [11] niet is meegenomen), alsmede het aantal geïncludeerde patiënten (N =12 - 2724) [9-14]. De referentiewaarde van hyperammoniëmie varieert met name bij de retrospectieve studies en de resultaten van deze studies moeten voorzichtiger geïnterpreteerd worden, omdat het niet altijd duidelijk is bij welke valproïnezuurgebruikers ammoniak is bepaald en waarom. Er is slechts één studie gevonden waarin wordt vergeleken met niet-valproïnezuurgebruikers [12].
Er zijn diverse risicofactoren geïdentificeerd voor het ontwikkelen van hyperammoniëmie bij valproïnezuur, waaronder dosering [6,8,10], co-gebruik van topiramaat [10,15] en leverenzyminducerende anti-epileptica zoals fenytoïne, fenobarbital, carbamazepine en oxcarbazepine [4-6,8,10,11]. Door de introductie van anti-epileptica als levetiracetam en het afnemen van het voorschrijven van enzyminducerende anti-epileptica over de jaren, is het vermoeden dat hyperammoniëmie bij valproïnezuurgebruik afneemt [11].
Klinische presentatie
Hyperammoniëmie kan leiden tot encefalopathie. Daling van het bewustzijn is een bekend symptoom bij een matige tot ernstige encefalopathie. Daarnaast zijn cognitieve (traagheid, geheugenproblemen), psychiatrische (hallucinaties, agitatie), motorische (flapping tremor, ataxie, vallen) en/of gastro-intestinale (misselijkheid) symptomen mogelijk [3].
Hyperammoniëmie bij valproïnezuurgebruik komt dus vaak voor, maar het ontwikkelen van encefalopathie is zeldzamer. In drie gevonden studies wordt encefalopathie beschreven bij 0,6 - 1.1% van de valproïnezuurgebruikers [6,8,10] (tabel 2). In twee andere grote retrospectieve studies werd bij 11/9608 (0,1%) en bij 20/793 (2,5%) valproïnezuurgebruikers encefalopathie vastgesteld [15,16].
In de meeste studies is de gevonden hyperammoniëmie mild [8,9,12]. Symptomen kunnen subtiel zijn waardoor de hyperammoniëmie niet wordt herkend. Daarnaast kunnen symptomen worden aangezien voor bijwerkingen van valproïnezuur zelf of aspecifiek zijn. Baddour et al. vonden bij valproïnezuurgebruikers zonder hyperammoniëmie meer ervaren symptomen dan bij gebruikers met hyperammoniëmie (64,9 ten opzichte van 43,2%) [14].
In deze casus was sprake van langer gebruik van valproïnezuur, ook jaren zonder klachten. Cognitieve problemen vielen als eerste op, maar er werd niet gedacht aan hyperammoniëmie. In de loop van het jaar ontstond uiteindelijk ook somnolentie overdag, waarschijnlijk door verdere stijging van het ammoniak. Hyperammoniëmie is beschreven na een enkele dosis [4,17], maar in de gevonden literatuur betreft het veelal chronisch gebruikers, met beschreven gemiddelde behandelduren van 1,5 tot 19 jaar [5,6,8,9]. Hypothese bij het verloop in deze casus is dat er al langer een mildere hyperammoniëmie was, en dat deze is toegenomen door veranderingen in het metabolisme door carnitinedepletie en veroudering.
Behandeling
De Koninklijke Nederlandse Maatschappij ter bevordering der Pharmacie (KNMP) schrijft dat valproïnezuur direct gestaakt moet worden bij hyperammoniëmie met neurologische symptomen, zoals braken, ataxie en verminderd bewustzijn [18]. Bij symptomen van lichtere aard en indien andere anti-epileptica een optie zijn, kan worden afgebouwd en geswitcht. Succesvolle behandeling van hyperammoniëmische encefalopathie met lactulose [14,19] en/of het suppleren van levocarnitine [2,14,20] is daarnaast beschreven in casuïstische mededelingen.
Conclusie
Hyperammoniëmie bij gebruik van valproïnezuur komt naar schatting voor bij 35% van de gebruikers. Routinematige controle van het plasma-ammoniak is volgens ons niet zinvol, omdat de hyperammoniëmie vaak mild en asymptomatisch verloopt en eventuele klachten alsnog op elk moment kunnen ontstaan, zoals in deze casus na jarenlang gebruik. Hyperammoniëmische encefalopathie is zeldzamer maar een gevaarlijke bijwerking. Ondanks de geschreven literatuur is deze bijwerking in onze ervaring bij veel clinici onbekend. Bij cognitieve en/of motorische achteruitgang dient men hierop alert te zijn en het ammoniaklevel te controleren.
Verantwoording
Geen belangenverstrengeling gemeld.
Literatuur
1. Bijl D. Naranjoscore: beoordeling oorzakelijk verband bijwerkingen. Ge-Bu 2011;45(11):132.
2. Nanau RM, Neuman MG. Adverse drug reactions induced by valproic acid. Clin Biochem. 2013 oct;46(15):1323-38.
3. Puijenbroek EP, Diemont WL, Grootheest van K. Application of Quantitative Signal Detection in the Dutch Spontaneous Reporting System for Adverse Drug Reactions. Drug Saf. 2003;26(5):293–301.Naranjo CA, et al. A method for estimating the probability of adverse drug reactions. Clin Pharmacol Ther 1981; 30: 239-245.Naranjo CA, et al. A method for estimating the probability of adverse drug reactions. Clin Pharmacol Ther 1981; 30: 239-245.Naranjo CA, et al. A method for estimating the probability of adverse drug reactions. Clin Pharmacol Ther 1981; 30: 239-245.
4. Chicharro AV, de Marinis AJ, Kanner AM. The measurement of ammonia blood levels in patients taking valproic acid: looking for problems where they do not exist? Epilepsy Behav. 2007 nov;11(3):361-6.
5. Rousseau MC, Montana M, Villano P, et al. Valproic acid-induced encephalopathy in very long course treated patients. Brain Inj. 2009 nov;23(12):981-4.
6. Tseng YL, Huang CR, Lin CH, et al. Risk factors of hyperammonemia in patients with epilepsy under valproic acid therapy. Medicine (Baltimore). 2014 sep;93(11):e66.
7. Ando M, Amayasu H, Itai T, Yoshida H. Association between the blood concentrations of ammonia and carnitine/amino acid of schizophrenic patients treated with valproic acid. Biopsychosoc Med. 2017 jul;11:doi:10.1186/s13030-017-0101-0
8. Duman B, Can KC, Ağtaş-Ertan E, et al. Risk factors for valproic acid induced hyperammonemia and its association with cognitive functions. Gen Hosp Psychiatry. 2019 jul-aug;59:67-72.
9. Holroyd S, Overdyke JT. Hyperammonemia Associated With Valproic Acid Use in Elderly Psychiatric Patients. J Neuropsychiatry Clin Neurosci. 2012;24(3):372-4.
10. Yamamoto Y, Takahashi Y, Suzuki E, et al. Risk factors for hyperammonemia associated with valproic acid therapy in adult epilepsy patients. Epilepsy Res. 2012 (sep);101(3):202-9.
11. Yamamoto Y, Takahashi Y, Imai K, Mishima N, Kagawa Y, Inoue Y. Changing incidence of hyperammonemia in Japan from 2006 to 2013: expansion of new antiepileptic drugs reduces the risk of hyperammonemia. Eur J Clin Pharmacol. 2015 dec;71(12):1517-24.
12. Adler LW, Regenold WT. Valproate-Related Hyperammonemia in Older Adult Psychiatric Inpatients. Prim Care Companion CNS Disord. 2015 apr;17(2):doi: 10.4088/PCC.14l01737
13. Tesen H, Katsuki A, Hori H, Atake K, Yoshimura R, Nakamura J. Plasma ammonia levels in patients treated with valproic acid. Neuropsychiatry. 2017:7(1);42-7.
14. Baddour E, Tewksbury A, Stauner N. Valproic acid–induced hyperammonemia: Incidence, clinical significance, and treatment management. Ment Health Clin. 2018 mar;8(2):73–7.
15. Noh Y, Kim DW, Chu K, et al. Topiramate increases the risk of valproic acid-induced encephalopathy. Epilepsia. 2013 jan;54(1):e1-4.
16. Lewis C, Tesar GE, Dale R. Valproate-Induced Hyperammonemic Encephalopathy in General Hospital Patients With One or More Psychiatric Disorders. Psychosomatics. 2017 jul-aug;58(4):415-20.
17. Ciftci S, Guler A, Deveci E, et al. A case with hyperammonemic encephalopathy triggered by single dose valproate. Neurological Sciences. 2016 dec;37(12):2017-18.
18. Informatorium Medicamentorum. Valproïnezuur [Internet]. Den Haag: Koninklijke Nederlandse Maatschappij ter bevordering der Pharmacie; 2020 apr 20 [geraadpleegd datum]. https://kennisbank.knmp.nl/article/Informatorium_Medicamentorum/S1470.html.
19. Wu MY, Chang FY, Ke JY, Chen CS, Lin PC, Wang TS. Valproic Acid-Induced Hyperammonemic Encephalopathy in a Patient with Bipolar Disorder: A Case Report. Brain Sci. 2020 Mar;10(3):187.
20. Mock CM, Schwetschenau KH. Levocarnitine for valproic-acid-induced hyperammonemic encephalopathy. Am J Health Syst Pharm. 2012 jan;69(1):35-9.
Referentie
Citeer als: Woudstra J, Schuur T, Meijler WJ, van Roon EN. Hyperammoniëmische encefalopathie door valproïnezuur bij een patiënt op de geheugenpolikliniek. Nederlands Platform voor Farmaceutisch Onderzoek. 2021;6:a1736.
DOI
https://www.knmp.nl/resolveuid/5089a4d8c9ea4f8e9c9d6178d82c0f67Open access



Reactie toevoegen