Acute, toxicologische screening wordt relevanter door uitbreiding van het standaardpanel van de drugs of abuse point-of-care test met gammahydroxyboterzuur en ketamine
- Rubriek: Oorspronkelijk artikel
- Identificatie: 2018;3:a1671
Kernpunten
- Met uitgebreide toxicologische screening van 100 patiënten werden bij 91 patiënten 234 geneesmiddelen of drugs gevonden die niet waren aangetoond met een drugs of abuse point-of-care test (DOA-POCT).
- Uitgebreide toxicologische screening was, in aanvulling op de routine DOA-POCT in urine, in 7% van de patiënten klinisch relevant voor het stellen van een juiste diagnose.
- Gammahydroxyboterzuur (GHB) en ketamine waren het meest relevant voor het stellen van de juiste diagnose.
Abstract
Acute, toxicological screening becomes more relevant by addition of GHB and ketamine to the standard test panel of the drugs of abuse point-of-care test
BACKGROUND
For diagnosis and treatment in the acute setting, it is crucial to know whether the patient’s clinical status might be explained by the effects of drugs.
OBJECTIVE
To determine how many drugs were detected by comprehensive toxicological screening, that could not be detected with a drugs of abuse point-of-care test (DOA-POCT). Furthermore, we determined in how many patients comprehensive toxicological screening did provide additional clinically relevant information on diagnosis and patient care, and which drugs were responsible for this.
DESIGN
In this prospective study, patients were included for whom a DOA-POCT was performed and residual urine and serum samples were available.
METHODS
DOA-POCTs were performed using the Triage TOX Drug Screen. Comprehensive toxicological screenings were performed using the Toxtyper LC-MSN method and two GC-FID methods for alcohols and gamma-hydroxybutyric acid (GHB), respectively. The clinical relevance of the comprehensive toxicological screening results on diagnosis and patient care decisions were quantified.
RESULTS
100 patients were included. Comprehensive toxicological screening identified 234 drugs in 91 patients that were not identified by DOA-POCT. On the other hand, DOA-POCT identified 34 DOA that were not identified by comprehensive toxicological screening. 7% of comprehensive toxicological screening results were found to be clinically relevant for the diagnosis, with GHB and ketamine being the drugs involved. Another 38% strengthened confidence in diagnosis and patient care decisions.
CONCLUSION
GHB and ketamine should be added to the panel of drugs we screen with the DOA-POCT in our acute, hospital setting.
Inleiding
Voor het stellen van een juiste diagnose en het starten van een juiste behandeling op de spoedeisende hulp (SEH) kan het relevant zijn om te weten of de klinische symptomen van een patiënt zijn te verklaren door het gebruik van drugs of abuse (DOA) en/of geneesmiddelen. Om hier snel uitsluitsel over te kunnen geven maakt het OLVG gebruik van de Triage TOX Drug Screen, een point-of-care test (POCT) die binnen 10 minuten een aantal drugs kan aantonen in urine [1-4]. In eerder onderzoek op onze SEH is aangetoond dat de klinische waarde van deze DOA-POCT in onze setting beperkt is, ondanks het snel beschikbaar zijn van de resultaten [3]. Wij vroegen ons af of dit komt door het beperkte aantal drugs dat kan worden aangetoond met het standaardpanel op de DOA-POCT, en de beperkte sensitiviteit van de DOA-POCT voor nieuwe designer drugs [1,2,5].
Dit onderzoek beoogde vast te stellen hoeveel middelen die niet met de DOA-POCT aan te tonen waren wel met een uitgebreide toxicologische screening worden aangetoond. Daarnaast hebben we onderzocht bij hoeveel patiënten een uitgebreide toxicologische screening aanvullende klinisch relevante informatie verschafte en welke middelen hiervoor verantwoordelijk waren.
Methoden
Setting en procedure
Het onderzoek werd uitgevoerd in het OLVG te Amsterdam. De SEH van het OLVG ontvangt op locatie Oost en West gezamenlijk zo’n 90.000 bezoekers per jaar. Hiermee is het een van de grootste SEH’s van Nederland waar relatief veel DOA-problematiek voorkomt.
Het onderzoek was prospectief van opzet: alle patiënten bij wie een arts een DOA-POCT liet uitvoeren in de periode juni 2016 tot september 2016 en bij wie voldoende spijturine en spijtserum beschikbaar was, werden geïncludeerd. Inclusie liep totdat er 100 patiënten waren geïncludeerd waarbij uitgebreide toxicologische screening kon plaatsvinden.
Tot aan uitgebreide toxicologische analyse werden spijturine en spijtserum bewaard bij –80°C. Serummonsters zijn maximaal gedurende twee weken opgeslagen geweest voor analyse. Urinemonsters zijn maximaal gedurende twee weken opgeslagen geweest voor analyse met gaschromatograaf-vlamionisatiedetector (GC-FID) en maximaal een jaar opgeslagen geweest voor analyse met de Toxtyper (TT).
Dit onderzoek is goedgekeurd door de medisch-ethische commissie van het OLVG en als niet-WMO-plichtig aangemerkt.
DOA-POCT
DOA-POCT in urine werd binnen een paar uur na afname uitgevoerd door het Hematologisch en Klinisch Chemisch Laboratorium met de Alere Triage TOX Drug Screen (Triage). Dit is een competitievebinding-immunoassay die elf verschillende drugs kan aantonen in urine (amfetamine, methamfetamine, opiaten, methadon, cocaïne, cannabis, barbituraten, benzodiazepines, tricyclische antidepressiva, fencyclidine en paracetamol). In het OLVG staat paracetamol uit op de test, waardoor er tien drugs in het panel worden gemeten [6].
Uitgebreide toxicologische screening
Uitgebreide toxicologische screening in spijturine en spijtserum werd uitgevoerd door het laboratorium van de ziekenhuisapotheek en omvatte:
• kwalitatieve toxicologische drugscreening met gevalideerde TT-methoden;
• kwantitatieve screening op gammahydroxyboterzuur (GHB) en alcoholen (ethanol, methanol, aceton, acetonitril en isopropylalcohol) met gevalideerde GC-FID methoden.
De TT is een LC-ESI-MSN: een ultra high performance vloeistofchromatograaf (UHPLC) gekoppeld aan een tandem-massaspectrometer (MSN) met ionenval. Als ionisatietechniek gebruikt de TT electrospray-ionisatie (ESI) [7-9]. De in dit onderzoek gebruikte bibliotheek was de Toxtyper 1.1-bibliotheek, waarin zo’n 900 DOA en geneesmiddelen zijn opgenomen. Daarnaast kunnen handmatig middelen worden toegevoegd, waaronder in ons geval 4-fluoramfetamine [10].
Als monstervoorbewerkingstechniek is eiwitprecipitatie toegepast [11]. Hierop zijn de TT-methoden in urine en serum gevalideerd in ons eigen laboratorium.
Gegevensanalyse
Primaire onderzoeksvraag was hoeveel middelen die niet met de DOA-POCT aan te tonen zijn wel met een uitgebreide toxicologische screening worden aangetoond. Om antwoord te geven op deze vraag zijn alle positieve resultaten van uitgebreide toxicologische screenings vergeleken met alle positieve resultaten van DOA-POCT’s. Het aantal extra gevonden middelen werd uitgedrukt in absolute getallen.
Secundaire onderzoeksvraag was bij hoeveel patiënten een uitgebreide toxicologische screening aanvullende (i.e. meer dan alleen DOA-POCT) klinisch relevante informatie verschafte en welke middelen hiervoor verantwoordelijk waren. Om antwoord te geven op deze vraag is de klinische waarde van uitgebreide toxicologische screening op diagnose en behandeling beoordeeld door een onafhankelijk expertpanel. Het expertpanel bestond uit een internist, een spoedeisende hulp arts en een ziekenhuisapotheker. Zij scoorden individueel, retrospectief de uitgebreide toxicologische screeningsresultaten op drie onderdelen, middels vijfpuntsschalen (tabel 1):
• diagnose;
• opname en monitoring;
• behandeling.
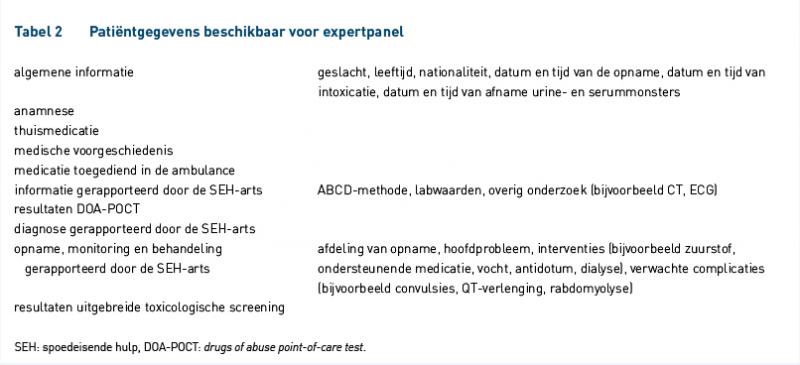
Deze schalen zijn afgeleid van schalen die zijn gebruikt in een onderzoek naar de klinische waarde van DOA-POCT op diagnose en behandeling [3]. Het expertpanel had de beschikking over informatie uit het elektronisch patiëntendossier (tabel 2).
De scores van de drie leden van het expertpanel zijn gemiddeld. Scores van 4 of 5 op een van de drie onderdelen (diagnose, opname en monitoring, of behandeling) werden beschouwd als klinisch relevant. Het aantal patiënten waarbij aanvullende klinische relevantie werd aangetoond werd uitgedrukt in een percentage. De verantwoordelijke middelen werden genoemd bij naam.
Analyse van de resultaten gebeurde met Excel 2010 en SPSS versie 22.0. Omdat EMV-waarden niet normaal verdeeld waren, werd gebruik gemaakt van de niet-parametrische Mann-Whitneytoets om significantie te toetsen.
Resultaten
In totaal zijn er 236 DOA-POCT-analyses uitgevoerd bij 235 patiënten. Bij 132 patiënten was geen of onvoldoende spijturine en/of spijtserum beschikbaar voor uitgebreide toxicologische screening, bij drie patiënten waren geen DOA-POCT-resultaten bekend en bij een patiënt waren twee DOA-POCT’s afgenomen binnen een ziekenhuisopname, hiervan hebben we er maar één meegenomen. De resultaten van 100 patiënten konden worden gebruikt voor analyse. In tabel 3 staan de patiëntkarakteristieken vermeld.
78 DOA-POCT waren positief voor ten minste één drug. In totaal werden 160 DOA aangetoond door DOA-POCT (tabel 4, rode kolom).
94 uitgebreide toxicologische screenings waren positief voor ten minste één middel in urine en/of serum. In totaal werden 360 DOA en geneesmiddelen aangetoond (169 DOA, 127 geneesmiddelen, 64 vluchtige stoffen). Van deze 360 aangetoonde DOA en geneesmiddelen waren er 234 (in 91 patiënten) niet aangetoond met DOA-POCT.
Wanneer alleen in urine was gekeken, dan waren 206 middelen gevonden (in 90 patiënten) die niet waren aangetoond met DOA-POCT. Wanneer alleen in serum was gekeken dan waren 161 middelen gevonden (in 80 patiënten) die niet waren aangetoond met DOA-POCT (figuren 1-3). Screenen in urine levert dus meer resultaat op dan screenen in serum, alhoewel de benzodiazepinen in urine vaker worden gemist.
De TT heeft 9 designer drugs (in 8 patiënten) aangetoond in urine en/of serum, allen amfetamine-achtigen, te weten 4-fluoramfetamine (4-FA: n = 4), benzodioxazoylbutanamine (BDB: n = 2), mefedron (n = 1) en methylon (n = 2). De DOA-POCT testte bij 4-FA en mefedron positief op amfetamine en negatief op methamfetamine. De DOA-POCT testte bij BDB en methylon negatief op zowel amfetamine als methamfetamine.
De TT vond 43 DOA in urine en/of serum die DOA-POCT niet vond (figuur 1). Het betrof 26 DOA die wel, en 17 DOA die niet in het panel van de DOA-POCT zitten (tabel 4, groene kolom, getallen met een * erachter). In figuur 1 staan 4-FA en mefedron ook weergegeven.
Andersom vond DOA-POCT 29 DOA die niet zijn teruggevonden met de TT (tabel 4, groene kolom, getallen met een † erachter ). Het betrof in 23 van de 29 gevallen dronabinol (THC, de metaboliet van cannabis).
Bij zeven patiënten (7%) waarbij een uitgebreide toxicologische screening was uitgevoerd was het expertpanel van mening dat de resultaten significant zouden hebben bijgedragen aan het stellen van de juiste diagnose (figuur 4: D4 + D5, n = 7). 5 van deze 7 patiënten hadden GHB gebruikt, waaronder een gecombineerd met cocaïne. Twee patiënten hadden ketamine gebruikt, waaronder een samen met methadon en een in combinatie met amfetamine en ethanol (tabel 5). In alle gevallen was GHB of ketamine de doorslaggevende factor voor het klinische beeld en de behandeling, waaruit kan worden geconcludeerd dat het aantonen of uitsluiten van deze drugs als klinisch relevant beschouwd mag worden.
In geen van de patiënten (0%) droegen de resultaten van de uitgebreide toxicologische screening significant bij aan het beleid rondom opname en monitoring, en de behandeling (figuur 4).
Ondanks dat de mediane EMV van de zeven patiënten waarbij uitgebreide toxicologische screening een klinische meerwaarde heeft opgeleverd flink lager was dan die van de overige patiënten, was dit verschil niet significant (Mann-Whitneytoets: P = 0,168; tabel 3).
Bij 38 patiënten (38%) versterkten de resultaten van uitgebreide toxicologische screening het vertrouwen in de diagnose (D3: n = 31), en/of opname en monitoring (M3: n = 4), en/of behandeling (B3: n = 14; figuur 4). Welke middelen hiervoor verantwoordelijk waren is te zien in tabel 5.
Beschouwing
In drie maanden tijd is bij 235 patiënten een DOA-POCT uitgevoerd. Dit grote aantal was meer dan bleek uit eerder eigen onderzoek [3,4]. Dit is te verklaren doordat:
• met de start van dit onderzoek de DOA-POCT weer extra onder de aandacht is gebracht bij de SEH artsen;
• de inclusie plaatsvond gedurende de zomermaanden wanneer er veel feesten worden georganiseerd in Amsterdam waar veel DOA worden gebruikt [12];
• het OLVG inmiddels uit twee locaties bestaat en dit onderzoek op de SEH van beide locaties is uitgevoerd.
Dit betrof een heel heterogene groep patiënten aangezien iedere patiënt met een intoxicatie in de differentiaaldiagnose kon worden geïncludeerd. Van dit grote aantal konden slechts 100 patiënten worden meegenomen, omdat in veel gevallen spijtmateriaal niet voorhanden was. De hectiek van de werkomgeving is hiervoor vermoedelijk de voornaamste reden. We hebben echter niet de indruk dat hierdoor onze resultaten beïnvloed zijn, omdat de patiëntkarakteristieken vergelijkbaar zijn.
Uitgebreide toxicologische screening in urine en/of serum leverde veel meer DOA en geneesmiddelen (234 extra) op dan DOA-POCT. Dit hadden wij ook verwacht aangezien de gebruikte TT-bibliotheek zo’n 900 middelen bevat, er tevens op GHB en alcoholen is gescreend en screening is uitgevoerd in zowel urine als serum. Van alle gevonden middelen in de uitgebreide toxicologische screening vond het expertpanel de resultaten alleen relevant voor het stellen van een juiste diagnose bij patiënten die amfetamine, cocaïne, ethanol, GHB, ketamine en methadon hadden gebruikt. Aangezien GHB of ketamine in alle gevallen de doorslaggevende factor was, zou uitbreiding van de drugsscreening met GHB en ketamine belangrijke extra informatie kunnen geven.
In totaal heeft de TT 47 amfetamine-achtigen aangetoond, waarvan 9 nieuwe designer drugs (19%). Hiervan werden er 4 gemist met de DOA-POCT. Bij 4-FA en mefedron testte DOA-POCT positief op amfetamine. In de Nederlandse drugsscene is zo’n 16% van de amfetaminen een nieuwe designer drug, wat door ons onderzoek wordt bevestigd [12,13].
De TT vond 26 keer een DOA in urine en/of serum die tot het panel van de DOA-POCT behoorde, maar niet werd aangetoond met DOA-POCT. 6 van deze 26 DOA werden door de TT enkel in serum gevonden en konden op de DOA-POCT dus ook niet in urine worden aangetoond. Bij de overige 20 kunnen er meerdere oorzaken ten grondslag liggen aan deze discrepantie. Allereerst zijn de detectiegrenzen van de TT en de DOA-POCT niet gelijk, waardoor een middel op de DOA-POCT niet, maar op de TT wel meetbaar is [14]. Daarnaast kan het bij de DOA-POCT voorkomen dat er een fout-negatief resultaat wordt geproduceerd wat inherent is aan de analysetechniek [1,2]. Tot slot blijkt de TT soms fout-positieve resultaten voor cocaïne in urine te geven door overdracht [14]. Dit kan het geval zijn geweest in 7 patiënten waarbij de DOA-POCT geen cocaïne aantrof en de TT wel.
Andersom vond de DOA-POCT 29 keer een DOA die niet werd aangetoond door de TT in urine en/of serum. Dit was een onverwacht resultaat. Aangezien de specificiteit van de Triage voor de meeste componenten >99% is [1,2], kan dit niet verklaard worden door mogelijke fout-positieve resultaten van de DOA-POCT. De specificiteit en sensitiviteit van de TT bleek uit recent onderzoek ≥97,7% voor amfetamine, methamfetamine, benzodiazepines, cocaïne, methadon en opiaten [14]. De sensitiviteit voor THC bleek daarin echter onvoldoende. Wanneer de 29 discrepanties nader bekeken worden, dan blijkt het in de meeste gevallen ook te gaan om THC die zowel in urine als in serum door de TT gemist zijn. Maar ook benzodiazepines werden regelmatig gemist door de TT, met name in urine. Bij de urinemonsters kan stabiliteit ook een rol hebben gespeeld, aangezien deze maximaal een jaar zijn bewaard voordat analyse met de TT heeft plaatsgevonden. THC-metabolieten vertonen een verval van ongeveer 30% en benzodiazepines lijken stabiel na een jaar bewaren bij –20°C [15,16]. Een andere mogelijkheid is dat ionsuppressie is opgetreden bij LC-ESI-MS van cannabinoïden. Voor cannabinoïden wordt bij voorkeur vastefase-extractie toegepast als monstervoorbewerkingstechniek, maar in dit onderzoek is eiwitprecipitatie toegepast [17,18]. Daarnaast zijn benzodiazepines in urine voornamelijk in geconjugeerde vorm aanwezig, welke wel reageren op de DOA-POCT maar niet tot de gebruikte TT-bibliotheek behoren [9,10,19].
Uitgebreide toxicologische screening in enkel urine vond meer DOA en geneesmiddelen (n = 206) dan uitgebreide toxicologische screening in enkel serum (n = 161). Psilocine (werkzame bestanddeel in hallucinerende paddenstoelen), methylon (amfetamine-achtige), amfetamine, cocaïne, analgetica (met name paracetamol) en cardiale middelen werden opvallend vaker aangetoond in urine dan in serum. Andersom werden benzodiazepines opvallend vaker aangetoond in serum dan in urine. Een verklaring hiervoor is dat de fase II-metabolieten (glucuronides) van benzodiazepines niet in de gebruikte TT-bibliotheek zaten [10,19]. Deze resultaten bevestigen dat screenen in urine de voorkeur geniet boven screenen in serum.
Uitgebreide toxicologische screening, in aanvulling op de routine DOA-POCT in urine, was in slechts 7% van de patiënten klinisch relevant voor het stellen van een juiste diagnose en in geen van de patiënten klinisch relevant bij het starten van een juiste behandeling. Wij hadden hier hogere percentages verwacht, aangezien de combinatie TT en GC-FID vrijwel alle DOA en geneesmiddelen vangt. Wel versterkten de resultaten in een behoorlijk aantal patiënten het vertrouwen van de arts in diagnose, opname en monitoring, en behandeling.
Een oorzaak voor de beperkte klinische waarde kan zijn dat uitgebreide toxicologische screening waarschijnlijk de meeste meerwaarde heeft bij onbegrepen intoxicaties terwijl in ons onderzoek een heel heterogene patiëntengroep is geïncludeerd. De DOA-POCT bleek uit eerder onderzoek het meest relevant bij patiënten met een onbegrepen daling van het bewustzijn en patiënten met psychiatrische en neurologische symptomen [3]. In ons onderzoek was de mediane EMV van de patiënten waarbij klinische meerwaarde is aangetoond ook 6 punten lager dan die van de overige patiënten. Hoewel dit verschil niet significant was, lijkt de klinische meerwaarde groter bij patiënten met een lagere EMV. Daarnaast meet de TT alleen kwalitatief. Aangezien behandeling bij overdosering met DOA gebeurt op basis van kliniek is het met name van belang te weten om welk type intoxicatie het gaat. Wel komt binnenkort een semi-kwantitatieve TT-bibliotheek beschikbaar.
Conclusie
Resultaten uit uitgebreide toxicologische screening met de combinatie TT en GC-FID (GHB en alcoholen) dragen bij SEH patiënten met een intoxicatie in de differentiaaldiagnose, in aanvulling op de routine DOA-POCT in urine, in geringe mate bij aan het stellen van een juiste diagnose. Aantonen van GHB en ketamine bleek met name relevant gevonden te worden voor dit doeleinde. Screenen op de aanwezigheid van GHB en ketamine in onze acute setting zou daarom een goede aanvulling kunnen zijn op onze huidige DOA-POCT. De betrouwbaarheid en de meerwaarde van een commercieel verkrijgbare GHB-sneltest op de SEH wordt daarom momenteel in het OLVG onderzocht.
Verantwoording
De auteurs willen de volgende personen bedanken voor hun bijdrage aan dit onderzoek: de leden van het expertpanel: prof. dr. D.J. Touw, ziekenhuisapotheker/klinisch farmacoloog, UMCG, Groningen; dr. C. Kramers, internist/klinisch farmacoloog, Radboudumc, Nijmegen; dr. M.H. Sandel, spoedeisende hulp-arts, OLVG, Amsterdam; en alle analisten van het laboratorium van de ziekenhuisapotheek, OLVG, Amsterdam.
Geen belangenverstrengeling gemeld.
Gebaseerd op het registratieonderzoek van J.A.J. van der Schaar.
Literatuur
1. Attema-de Jonge ME, Peeters SYG, Franssen EJF. Performance of three point-of-care urinalysis test devices for drugs of abuse and therapeutic drugs applied in the emergency department. The Journal of Emergency Medicine. 2012;42(6):682-691.
2. Attema-de Jonge ME, Peeters SYG, Franssen EJF. Betrouwbaarheid van drie sneltests voor drugs of abuse op de spoedeisende hulp. Pharmaceutisch Weekblad: Wetenschappelijk Platform. 2008;2(7):146-149.
3. Lager PS, Attema-de Jonge ME, Gorzeman MP, Kerkvliet LE, Franssen EJF. Toxicologische screeningstests voor drugs of abuse beïnvloeden de diagnose maar hebben beperkte invloed op de behandeling. Pharmaceutisch Weekblad: Wetenschappelijk Platform. 2013;7:2-5.
4. Choo WP, Gorzeman MP, Attema-de Jonge ME. Sneltest voor drugs of abuse op de spoedeisende hulp: twee jaar ervaring. Pharmaceutisch Weekblad: Wetenschappelijk Platform. 2011;5:86-90.
5. Attema-de Jonge ME en Malingré MM. Sneltest op SEH: handig, maar ook beperkt. Pharmaceutisch Weekblad. 2009;26:20-23.
6. Alere Triage. TOX Drug Screen Product Insert. 2016.
7. Toxtyper™ – a comprehensive LC-MSn application for clinical research and forensic toxicology [internet]. Bruker: application note # LCMS-91. Beschikbaar op: https://www.bruker.com/fileadmin/user_upload/8-PDF-Docs/Separations_MassSpectrometry/Literature/literature/ApplicationNotes/1828629_AppNote_LCMS-91_Toxtyper_2014_ebook.pdf [geraadpleegd juli 2017].
8. Comprehensive detection and identification of synthetic cannabinoids using the Toxtyper platform [internet]. Bruker: application note # LCMS-99. Beschikbaar op: https://www.bruker.com/fileadmin/user_upload/8-PDF-Docs/Separations_MassSpectrometry/Literature/ApplicationNotes/LCMS-99_Toxtyper_SynthCannabinoids_01-2015_eBook.pdf [geraadpleegd juli 2017].
9. Interlaboratory tests demonstrate the robustness and transferability of the Toxtyper™ workflow [internet]. Bruker: application note # LCMS-92. Beschikbaar op: https://www.bruker.com/fileadmin/user_upload/8-PDF-Docs/Separations_MassSpectrometry/Literature/literature/ApplicationNotes/1828632_AppNote_LCMS-92_Toxtyper_InterlaboratoryTests_2014_ebook.pdf [geraadpleegd juli 2017].
10. Bruker. Toxtyper 1.1 Libraries Reference Manual. Revision 2 (May 2014).
11. Bruker. Toxtyper 1.1. User tutorials for the Toxtyper automated analysis solutions. Revision 2 (June 2014).
12. Trimbos Instituut. Nationale Drug Monitor. Jaarbericht 2016.
13. Trimbos Instituut. Drugs Informatie en Monitoring Systeem (DIMS). Jaarbericht 2016.
14. Ott M, Berbalk K, Plecko T, Wieland E, Shipkova M. Detection of drugs of abuse in urine using the Bruker ToxtyperTM: experiences in a routine clinical laboratory setting. Clinical Mass Spectrometry. 2017;4-5:11-18.
15. Mata DC. Stability of 26 sedative hypnotics in six toxicological matrices at different storage conditions. Journal of Analytical Toxicology. 2016;40:663-668.
16. Desrosiers NA, Lee D, Scheidweiler KB, Concheiro-Guisan M, Gorelick DA, Huestis MA. In vitro stability of free and glucuronidated cannabinoids in urine following controlled smoked cannabis. Analytical and Bioanalytical Chemistry. 2014;406(3):785-792.
17. Dams R, Huestis MA, Lambert WE, Murphy CM. Matrix effect in bio-analysis of illicit drugs with LC-MS/MS: influence of ionization type, sample preparation and biofluid. Journal of The American Society for Mass Spectrometry. 2003;14:1290-1294.
18. Sørensen LK en Hasselstrøm JB. Sensitive determination of cannabinoids in whole blood by LC-MS-MS after rapid removal of phospholipids by filtration. Journal of Analytical Toxicology. 2017;41:382-391.
19. Wissenbach DK, Meyer M, Remane D, Philipp AA, Weber AA, Maurer HH. Drugs of abuse screening in urine as part of a metabolite-based LC-MSN screening concept. Analytical and Bioanalytical Chemistry. 2011;400:3481-3489.
Referentie
Citeer als: Van der Schaar JAJ, Attema-de Jonge ME, Gresnigt FMJ, Franssen EJF. Acute, toxicologische screening wordt relevanter door uitbreiding van standaardpanel van de drugs of abuse point-of-care test met GHB en ketamine. Nederlands Platform voor Farmaceutisch Onderzoek. 2018;3:a1671.
DOI
https://www.knmp.nl/resolveuid/44b9af66d96746998b1ef9b484691caeOpen access









Reactie toevoegen